
对脑梗死损伤机制的研究大多集中在缺血缺氧对神经元的影响,大量研究表明,缺血缺氧损伤可诱导神经元大量释放谷氨酸,导致谷氨酸在细胞外液大量蓄积,引起谷氨酸的毒性作用,被认为是脑梗死损伤的主要机制。而近年的研究表明,星形胶质细胞也能够释放谷氨酸,参与神经系统的谷氨酸代谢。提示缺血缺氧损伤也有可能诱导星形胶质细胞释放谷氨酸,从而加重谷氨酸的毒性作用。
本研究通过原代培养星形胶质细胞,采用氧气葡萄糖剥夺( oxygen glucose deprivation,OGD) 模型体外模拟缺血缺氧损伤环境,观察 OGD 刺激对星形胶质细胞谷氨酸释放的影响。此外,由于连接子蛋白43( connexin 43,Cx43) 半通道是星形胶质细胞释放谷氨酸的主要途径,本研究还探讨了 Cx43 半通道是否参与了 OGD 诱导的谷氨酸释放。通过上述研究,以期探讨脑梗死中枢神经系统损伤的机制,为脑梗死的临床治疗提供新的思路。
1 材料和方法
1. 1 材料
胎牛血清 ( fetal bovine serum,FBS) 、DMEM 液为Invitrogen 公司产品; 小鼠抗胶质纤维酸蛋白 ( glial fibrillaryacidic protein,GFAP) 抗体及兔抗 Cx43 多克隆抗体均为 Sigma公司产品; 兔抗 β-Ⅲ微管蛋白( β-Ⅲ tublin) 抗体为Promega公司产品; 荧光二抗购自 Jackson 公司; Gap26 为Severn Biotech公司产品; Cx43 反义寡核苷酸( antisense oligodeoxynucleotide,ASODN) 由 Sangon Biotech 公司合成; 高效液相色谱仪购自Waters 公司; 激光共聚焦显微镜购自 Lecia 公司; 新生大鼠购自解放军总医院第一附属医院实验动物中心。
1. 2 方法
1. 2. 1 细胞培养 培养方法参见文献[3],具体方法如下:取新生 1 d 的 SD 大鼠,无菌取得脑组织,分离血管和脑膜后,将脑组织剪成小块,1.25 g/L 胰酶消化后,用含100 mL/L FBS的 DMEM 液终止消化,将细胞悬液种入预先铺有多聚赖氨酸的培养瓶中,密度为2.0 ×105个/cm2,于 37℃、50 mL/L CO2培养箱培养,每 3 d 换液 1 次。10 d 后,在 37℃恒温摇床上240 r / min 振荡 24 h,弃上清液。用 1. 25 g / L 胰蛋白酶消化后种植入涂有多聚赖氨酸盖玻片的 24 孔培养板,种植密度1. 0 × 105个/cm2。简要步骤如下: 多聚甲醛固定后,加入小鼠抗 GFAP 抗体( 1∶1 500) 或兔抗 β-Ⅲ tublin( 1∶1 000) 过夜;而后加入 FITC 标记的抗小鼠 IgG 或 FITC 标记的抗兔 IgG( 1∶500) ,结果显示,星形胶质细胞的含量 > 90%,并且不含有神经元。2 ~4 周传代后,星形胶质细胞用于实验。
1. 2. 2 实验分组和缺糖缺氧刺激 星形胶质细胞随机分为4 组: 正常对照组、OGD 刺激组、Gap26( Cx43 半通道阻断剂)联合 OGD 刺激组、Cx43-ASODN 联合 OGD 刺激组。对于Gap26 联合 OGD 刺激组,在刺激前,预先将星形胶质细胞与300 μmol / L Gap26 ( VCYDKSFPISHVR ) 共 孵 育 2 h; 对 于Cx43-ASODN联合 OGD 刺激组,同样预先将星形胶质细胞与Cx43-ASODN 共孵育 2 h。Cx43-ASODN 依据序列 5'-ACTC-CAGTCACCCAT-3' 而合成,它可以有效的抑制 Cx43 的表达。
缺糖缺氧损伤模型方法如下: 将星形胶质细胞培养7 ~ 9 d 后,将培养基置换成不含糖和氧的培养基,置于 37℃ 、950 mL / L N2、50 mL/L CO2、饱和湿度的培养环境下培养。
分别培养 0、15、30、60、90、120 min。每一培养时段各设6 个平行样本( n = 6) 。
1. 2. 3 细胞外液谷氨酸测定 在每个刺激时间点,提取细胞培养液,离心 4 min 后,取上清,采用高效液相色谱( highpressure liquid chromatography,HPLC) 来测定细胞外液谷氨酸浓度。具体方法详见文献。
1. 2. 4 免疫荧光染色测定星形胶质细胞 Cx43 和 GFAP 的表达情况 各组细胞用 40 g/L 多聚甲醛液固定 30 min( 室温) ,吸出固定液,0. 01 mol/L PBS 洗 3 次。星形胶质细胞培养孔中加入小鼠抗 GFAP 单克隆抗体( 1∶1 500) 和兔抗 Cx43 多克隆抗体( 1∶1 500) 混合液,4℃过夜,而后星形胶质细胞换为与第一抗体相应的结合了荧光素的二抗混合液,避光孵育 2 h,0. 01 mol / L PBS 洗 3 次后,800 mL / L 甘油封片,激光扫描共聚焦显微镜观察结果。
1. 2. 5 统计学分析 各组数据以 x ± s 表示,采用多个样本均数比较的方差分析及多重比较的 LSD-t 检验进行统计学分析。P <0. 05 认为差异具有统计学意义。
2 结果
2. 1 OGD 升高细胞外液谷氨酸浓度 采用 HPLC法,测定了不同时间点细胞外液的谷氨酸浓度。结果发现,正常状态下( 0 min) ,细胞外液谷氨酸浓度大致为( 2. 43 ±0. 17) nmol/mL。而 OGD 刺激后,细胞外谷氨酸浓度逐渐升高,并在刺激 90 min 后,达到峰值,为( 5. 00 ± 0. 30) nmol/mL,显着高于对照组,差异有统计学意义( P <0. 05) 。该结果表明,缺糖缺氧刺激可以显着升高细胞外液谷氨酸水平,说明缺糖缺氧刺激可以促进星形胶质细胞释放谷氨酸。【表1】

2. 2 缺糖缺氧损伤诱导星形胶质细胞表达 Cx43 蛋白 在星形胶质细胞膜上,Cx43 蛋白构成 Cx43 半通道,是星形胶质细胞释放谷氨酸的主要通路之一。
本研究探讨了 OGD 刺激对细胞 Cx43 蛋白的影响。
通过免疫荧光染色发现,对照组 Cx43 蛋白的平均荧光强度 ( mean fluorescence intensity,MFI) 为( 80 ±28) 自由单位 ( arbitrary unit,AU) 。OGD 刺激后,Cx43 蛋白表达的信号强度明显升高,在刺激60 min后,其 MFI 达峰值,为( 158. 00 ± 43. 00) AU,显着高于对照组( 图 1) 。说明 OGD 刺激可诱导星形胶质细胞表达 Cx43,为谷氨酸的进一步释放提供了通路。OGD 刺激也能促进 GFAP 的表达,GFAP 的信号强度也明显升高,刺激 60 min 时,对照组为( 98. 00 ±24. 00) AU; OGD 刺激组为( 170. 00 ± 34. 00) AU,说明缺糖缺氧刺激也激活了星形胶质细胞。【图1.略】
2. 3 Cx43 半通道阻断剂 Gap26 能够抑制缺糖缺氧刺激诱导的谷氨酸释放 Gap26 是特异性的 Cx43 半通道阻断剂,本实验采用 Gap26 阻断 Cx43 半通道,以探讨 Cx43 半通道在缺糖缺氧刺激诱导谷氨酸释放中的作用。
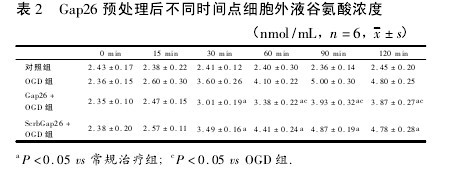
Gap26 预处理星形胶质细胞后,经过缺糖缺氧刺激,细胞外液谷氨酸浓度显着低于单纯缺糖缺氧刺激组( 表 2) 。在刺激 90 min 后,细胞外液谷氨酸浓度为( 3. 93 ±0. 32) nmol/mL,比单纯 OGD 刺激组减少了 50%( P <0. 05) 。说明 OGD 刺激下,星形胶质细胞通过 Cx43 半通道释放谷氨酸。此外,还发现Gap26 预处理后,OGD 刺激 60、90、120 min 后,细胞外液谷氨酸浓度还是高于对照组,说明 Cx43 半通道也并非唯一的释放途径。此外,为排除 Gap26 的非特异性反应,本研究还选用了乱序 Gap26 肽段( scrambled Gap26 peptide,Scrb Gap26) 来预处理星形胶质细胞,Scrb Gap26 预处理后,给予缺糖缺氧刺激,细胞外液谷氨酸浓度与单纯缺糖缺氧刺激组间无显着性差异( P >0. 05,表 2) 。【表2】
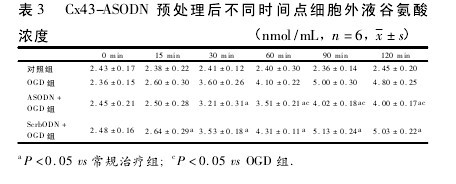
2. 4 Cx43 特异性反义寡核苷酸( Cx43-ASODN) 能够阻断缺糖缺氧刺激诱导的谷氨酸释放 既往研究表明,应用 Cx43 特异性 ASODN 可以暂时性敲除Cx43 蛋白,从而阻断了 Cx43 半通道的形成。本研究发现,采用 Cx43-ASODN 抑制 Cx43 表达后,缺糖缺氧刺激 60、90、120 min 后,细胞外液谷氨酸浓度显着低于单纯缺糖缺氧刺激组。刺激 90 min 后,细胞外液谷氨酸浓度为( 4. 02 ± 0. 18) nmol/mL,显着低于单纯缺糖缺氧组的( 5. 00 ± 0. 30) nmol/mL( P <0. 05) 。同样,为排除 ASODN 的非特异性反应,我们还选用了乱序 ODN 作为阴性对照。结果表明,乱序 ODN 对于谷氨酸的释放没有影响。【表3】
3 讨论
谷氨酸的兴奋性毒性作用在脑梗死的神经功能损害中起到了非常关键的作用。脑梗死期间,神经元通过突触末梢释放大量的谷氨酸至突触间隙,同时突触后膜和星形胶质细胞对谷氨酸再摄取作用减弱,致使细胞外液大量的谷氨酸聚集,过度刺激突触后膜的谷氨酸受体引起神经元持续去极化,从而干扰神经元的功能。
星形胶质细胞通常被认为对神经元具有支持和保护作用,但同时对细胞外液谷氨酸的浓度也具有调节功能。主要调节方式为通过谷氨酸转运体( functional glutamate transporters) 将细胞外液的谷氨酸转运至细胞内。但近年研究发现,星形胶质细胞也能够主动释放谷氨酸。本研究结果表明,缺糖缺氧刺激后,细胞外液谷氨酸浓度显着增高,这提示:缺糖缺氧促进星形胶质细胞谷氨酸的释放,这可能是脑梗死时谷氨酸毒性作用的另一机制。星形胶质细胞主动释放谷氨酸的途径很多,其中最为主要的有以下几种方式: 谷氨酸再摄取转运体逆向转运、与胞吐偶联的 Ca2 +依赖性谷氨酸释放、阴离子释放通道、功能性 pannexin1 通道、嘌呤受体介导的谷氨酸释放、Cx43 半通道。在本研究中,我们仅探讨了 Cx43 半通道在缺糖缺氧环境中的作用。研究结果表明,缺糖缺氧环境下,Cx43 半通道参与了谷氨酸的释放。此外还发现,缺糖缺氧环境下,Cx43 表达的峰值( 60 min) 先于谷氨酸释放的峰值( 90 min) ,这是因为 Cx43 蛋白自内质网合成后,只有通过高尔基体转运至细胞膜表面,才能发挥其功能,形成功能性半通道,因此存在一定的“时间差”。
当然,本研究并不能排除其他方式的释放途径。
例如,最近的研究就发现,缺糖缺氧刺激能够诱导嘌呤受体 P2X7 的表达,提示嘌呤受体也可能参与了缺糖缺氧诱导的谷氨酸释放。此外,OGD 损伤也可以降低星形胶质细胞谷氨酸转运体的表达,这将间接导致谷氨酸在细胞外液的蓄积。这些潜在的机制就解释了为什么阻断 Cx43 半通道只能部分而非完全抑制 OGD 诱导的细胞外液谷氨酸浓度的升高。
Cx43 半通道由 3 个缝隙连接蛋白构成,在中枢神经系统,主要表达于星形胶质细胞。Cx43 在中枢缺血缺氧损伤中的作用,目前还尚存在争论。一般认为,Cx43 半通道可以迅速的传递损伤或死亡信息至周围的细胞,导致周边区细胞出现凋亡或死亡,即缝管连接介导的旁观者效应( gap junction-mediatedbystander effect)。对于海马急性梗死大鼠,抑制Cx43 蛋白表达可以增加海马区存活神经元的数量,并且提高大鼠的神经功能学评分。但也有研究发现,Cx43 半通道可以将一些有益的神经营养因子、递质或第二信使传递至周边细胞,从而产生一系列神经保护作用( good samaritan effect)。但究竟是哪种效应占据上风,还要视损伤时间和损伤程度而定。
总之,本研究发现,缺糖缺氧刺激可以诱导星形胶质细胞通过 Cx43 半通道释放谷氨酸,可能进一步加重了缺糖缺氧损伤所致的谷氨酸毒性作用,这为缺血缺氧性脑损伤的治疗提供了新的途径。
参考文献:
[1]Ye HB,Shi HB,Yin SK. Mechanisms underlying taurine protectionagainst glutamate-indeced neurotoxicity[J]. Can J Neurol,2013,40( 5) : 628 -634.
[2]Kostandy BB. The role of glutamate in neuronal ischemic injury: therole of spark in fire[J]. Neurol Sci,2012,33( 2) : 223 - 237.
[3]Jiang S,Yuan H,Duan L,et al. Glutamate release through connexin43 by cultured astrocytes in a stimulated hypertonicity model[J].Brain Res,2011,1392( 5) : 8 - 15.
[4]O’Carroll SJ,Becker DL,Davidson JO,et al. The use of connexin-basedtherapeutic approches to target inflammatory diseases[J]. MethodsMol Biol,2013,1037( 1) : 519 - 546.
[5]廖春华,吴中亮,赵 钢. Cx43 对大鼠急性水中毒后脑水肿的影响[J]. 第四军医大学学报,2008,29( 13) : 1226 -1228.
[6]吴中亮,廖春华,任 宁. 缝隙连接蛋白 43 与创伤后脑水肿相关性研究[J]. 中华神经外科疾病研究杂志,2008,7( 3) : 201 -204.





