摘 要: 近年来,由于金纳米粒子独特的物理化学性质以及良好的生物相容性和生物安全性,吸引越来越多的科研工作者对其展开广泛的研究和开发。从金纳米粒子的合成方法、特性以及应用开发等方面的对金纳米粒子近年来的研究进展进行了比较详细的综述。
关键词: 金纳米粒子; 合成方法; 应用开发;
Abstract: In recent years, more and more researchers have been attracted to carry out extensive research and development on gold nanoparticles due to their unique physical-chemical properties,good biocompatibility and biosafety. In this paper, the recent research progress of gold nanoparticles was reviewed in detail from the synthetic methods, properties and application development.
Keyword: Gold nanoparticles; Synthetisis method; Application development;
金是一种化学性质非常稳定的金属,常用于装饰和货币,但当其尺寸缩小至纳米级别时性质会发生奇特的变化。金纳米粒子由于具有小尺寸效应、表面效应、量子尺寸效应和宏观量子隧道效应等,会产生不同于块体金的特殊物理化学性质。
1 、金纳米粒子的性质
1.1 、表面等离子共振特性
在一束波长远大于金纳米粒子的入射光的影响下,金纳米粒子中的电子重新分布,产生库仑力,在方向相反的内外电场共同作用下其自由电子集体震荡发生共振的现象,即表面等离子共振(SPR)。表面等离子共振会在共振波长处产生强烈的散射峰和吸收峰,而表面等离子共振的散射峰和吸收峰性质则取决于金纳米粒子的形貌与大小,是人工调节金纳米粒子光学性质的重要手段。

1.2 、荧光特性
金纳米粒子在适当波长的光照照射给予一定激发能量时,本身出现一定的原生荧光[1]。而在金纳米粒子被芘基、聚辛基和苯硫基等特定基团修饰包覆后,由于共振能量的迁移会具有荧光特性[2]。金纳米粒子的荧光强度则与纳米颗粒大小和包覆基团种类有关。
1.3 、电化学特性
由于金纳米粒子的分隔导带与满带的禁带具有一定间隙,当金纳米粒子的尺寸小到某一程度时产生量子尺寸效应,导带与禁带带隙变宽,使其从导体向绝缘体转换。经过对有机单分子层保护的金纳米粒子的研究发现,金纳米粒子的表面存在双电层电容,其作用可看作一个纳米尺寸的电极,其双电层电容的值会随着金纳米粒子表面包覆的烷基链长度的减小而增加。
1.4、 分子识别特性
金纳米粒子的可控组装是其进行分子识别的基础。金纳米粒子可通过氢键、范德华力、抗原-抗体等作用下选择性修饰上特异分子识别官能团。当其与对应分子相接触时会诱导超分子结构形成,其紫外可见光谱、荧光光谱等谱图中代表识别体的特征峰会发生变化,进而识别检测受检分子。
2 、金纳米粒子的制备
不同形态的金纳米粒子的性质也有很大差异,人们采用多种方法可控合成不同尺寸,形貌的金纳米颗粒,如金纳米球、金纳米棒、金纳米笼等。下面介绍几种主要的金纳米粒子合成方法。
2.1 、柠檬酸钠还原法
该法是1951年TURKEVITCH[3]最早提出粒径可控的制备纳米金的方法,至今仍是合成金纳米粒子常用的方法之一。制备原料只需3种:氯金酸、柠檬酸钠和超纯水。在水溶液高温条件下,柠檬酸钠作为还原剂也是稳定剂可制备不同粒径的纳米金。该法多用来制备粒径在100 nm以下的球状纳米金,但无法制备太小的金纳米粒子。
2.2 、晶体种子生长法
晶种生长法可以使人们对金纳米粒子的形状、尺寸、组成和结构等方面进行控制合成。南卡罗莱纳大学的Murphy课题组[4]在2001年首次提出可以用尺寸较小的金胶体颗粒作为种子合成棒状金纳米粒子。该法分为成核和生长两步进行,首先通过化学还原法制备出微小的金纳米粒子作为晶种,然后将晶种置于添加了不同比例还原剂、表面稳定剂等溶液的生长液中,使生长液中的游离态的Au3+不断被还原为零价的Au原子并在晶种上定向沉积,最终形成各种不同尺寸、形态的金纳米粒子。生长液的不同配比和晶种的添加比例都是控制金纳米粒子大小和形状的关键。
2.3、 两相法
1994年BRUST[5]等提出通过两相法合成金纳米颗粒,该法与其他的方法相比,在合成较小粒径粒子时具有较大的潜力。在水相和有机相的混合液中利用表面活性剂将水相中的游离态Au3+离子转移到有机相中,再通过还原剂和硫醇稳定剂将Au3+还原为Au原子并由硫醇包覆保护起来。由该法制得的金纳米粒子稳定性很好且易于进行修饰。
2.4 、模板法
MARTIN[6]首次报道将游离的金纳米离子沉积到作为模板的多孔氧化铝薄膜上制得金纳米颗粒。过程是以介孔或微孔的纳米材料为模板,结合化学沉积或电化学沉积等技术将游离的金离子还原、沉积在模板的孔壁上,最后再用溶解、烧结、蚀刻等方法去除模板,形成形貌各样的金纳米粒子。利用该法得到的金纳米粒子更利于控制形状和尺寸,具有良好的均一性。
2.5 、电化学法
该方法最早由WANG[7]等提出用以制备金纳米粒子。首先是将金板作为阳极,在通电下,牺牲阳极电极,产生金离子,以铂板作为阴极将金离子还原,以表面活性剂十六烷基三甲基溴化铵(CTAB)和四正十二烷基溴化铵的混合溶液作为电解液,在超声及控制电流稳定的条件下进行电解。这种方法便于通过改变沉积时间、电压、电流等条件来控制金纳米粒子大小,制得的金纳米颗粒粒径均一,但耗能较大,生产成本高。金纳米粒子的制备方法除上述几种之外还有光化学法、自组装法、生物还原法以及一些特殊的物理方法等,它们都可以制备出各式各样的金纳米粒子。
3、 金纳米粒子的应用
3.1 、癌症光热疗法领域的应用
近年来,癌症已经成为严重威胁人类健康的重大疾病。而现有的癌症临床治疗方法有化疗、放疗和手术疗法等,它们都具有强烈的毒副作用和局限性。在这个背景下,空间定位精准且对患处周围细胞组织损伤较小的光热治疗就进入了人们的视野。光热治疗是利用光热材料将光能高效的转化为热能,进而升高肿瘤组织的温度,以达到杀死肿瘤细胞的目的。金纳米粒子在红外光的照射下因其独特的表面等离子体共振(SPR)特性而具有显着的光热转换效应,同时又因为金纳米粒子具有良好的生物相容性,因此在癌症的光热治疗方面具有非常好的应用前景。
图1 光热疗法原理图[8]
![图1 光热疗法原理图[8]](http://www.xueshut.com/uploads/allimg/201207/36-20120G01TQ44.jpg)
ALI MOUSTAFA[9]教授团队将棒状金纳米粒子的尺寸、表面改性、浓度和等离子体光热疗法的激光功率进行优化,使其进行光热效应对癌细胞的死亡作用达到最大。同时进行了金纳米棒在体内15个月的毒性研究,证明了该金纳米棒平台在小鼠的癌症治疗中是安全有效的。CHEN[10]等制备了聚乙烯亚胺(PEI)改性的金纳米棒,然后通过静电作用于双核甘酸(Cp G)结合,最后再被巨噬细胞吞噬用于癌症的光热和免疫治疗,其中巨噬细胞可提供体内长循环和肿瘤组织靶向作用,而肿瘤组织在近红外光照后可产生原位肿瘤特异性抗原,进一步增强人体的特异性免疫。该法联合了光热治疗和人体免疫系统,对恶性癌症提供新的治疗方法。
3.2 、在药物载体领域的应用
许多药物由于其水溶性差、p H敏感等问题而不能直接使用,需要载体将其运输至作用部位。纳米药物载体选用合适的纳米材料对药物成分进行包裹,用于调控其在体内释药速度和生物透过性,可以大大提高药物的利用率[11]。由于金纳米粒子尺寸和形貌可控、生物相容性好、比表面积大、表面易修饰等优点,且同时具有独特的光热效应,在癌症治疗方面不仅能协同进行光热治疗,而且还是很好的药物载体。除药物以外这个载药体系还可通过负载各种功能分子使其载体赋予p H响应性[12]、靶向性[13]等特点。盐酸阿霉素(DOX)作为治疗实体瘤最为有效的药物之一,在临床上也常被用来治疗多种类型癌症,但此药物对病变部位生物利用度低,特异性差,且具有全身毒副作用,极大地限制了药物的治疗剂量,为此FENG[14]等利用双端巯基聚乙二醇(HS-PEG-SH)将金纳米颗粒自组装成金纳米团簇,并将通过化学结构修饰的p H敏感性的阿霉素装载其中。该载体系统具有优良的脑肿瘤靶向能力,且血液循环时间较长,在保持高浓度一段时间之后,可以被机体快速清除而避免造成生物毒性。PENG[15]等制备不同粒径的负载阿霉素金纳米颗粒的载药系统,验证大小对药物癌症治疗的影响。结果表明,尺寸小于6 nm能够经肾脏清除的纳米载药体系具有显着的肿瘤靶向和高效的药物渗透性,有望成为一种高效的递药手段。
3.3 、在CT成像领域的应用
计算机断层扫描(Computed Tomography,CT)是临床应用非常广泛的无创成像检查设备,具有适用范围广、扫描速度快、价格相对低廉等优点。由于人体有些软组织的密度相近,图像对比度较差,为了更准确地诊断疾病,临床使用时会给患者注射大剂量的CT造影剂,而最早也是最多使用的造影剂就是碘化合物,这种小分子造影剂在人体循环时间较短,缺乏组织特异性,高浓度时甚至对肾脏具有毒副作用,这些缺点限制了它的进一步发展。
LU[16]等设计合成了一种由树状大分子稳定的金纳米粒子和超小Fe3O4粒子复合而成的新型种子纳米颗粒,并通过可控调节生长形成稳定的纳米金花包埋超小铁纳米粒子多功能纳米平台。该平台优于单纯金纳米颗粒的光热转换效率,具有良好的X-射线衰减特性,实现了肿瘤的T1的MR/CT/PA多模态成像导引的PTT/RT联合治疗应用。TSVIRKUN[17]等通过对金纳米颗粒表面修饰靶向半胱氨酸组织蛋白酶的探针ABPs,研制出了首例CT成像检测酶活性的探针。而组织蛋白酶的丰度、活性和许多肿瘤的发展进程密切相关,靶向其活性的功能性成像,将生理过程和成像信号直接联系起来,有望应用于临床诊断中。
3.4 、在抗菌领域的应用
抗生素的发现和应用是人类历史的一大革命,但随着其在临床上广泛应用,病菌耐药性的问题也越来越严重。抗生素药物的误用、滥用使致病菌很快产生了耐药性,再次感染时只会摄入更多的抗生素,病菌也会产生更强的耐药性,以此恶性循环下去致使病菌将产生无可比拟的耐药性,即所谓的超级细菌。终将有一天人们将面对无药可用的局面。因此寻找新的抗菌手段是医药研发领域的紧急课题,而纳米金特殊的理化性质则为抗菌方法提供了新的思路。纳米金粒子本身具有抗菌效应,拥有良好的生物相容性,可作为载体协同其他抗菌药物高效抑菌灭菌。纳米金粒子表面等离子共振特性更是在此基础上赋予其光热效应,通过局部的红外照射升温达到杀菌的效果。HUO[18]等在阳离子金纳米颗粒中引入两性配体合成基于两性金纳米颗粒的抗菌剂。实验证明,通过调控金纳米颗粒的内核尺寸可以轻松控制其抗菌活性,随着内核尺寸的增加以及电荷取向的变化,颗粒的抗菌活性会急剧地增加。HU[19]等针对毒性很强的耐甲氧西林金黄色葡萄球菌(MRSA)设计了一种表面适应性的金纳米粒子。利用正常组织和耐甲氧西林金黄色葡萄球菌生物膜的p H差异,将混合的两性带电离子自组装单层修饰在金纳米粒子表面,使其在正常组织中快速扩散,而在酸性病菌生物膜的表面聚集,聚集的金纳米粒子具有较强的近红外吸收率,在局部红外照射下表现良好的光热效应,热消融MRSA生物膜并对正常组织没有损伤。由于这种p H响应型的金纳米粒子不负载抗生素,在治疗抗药性细菌感染方面具有很大的潜力。
3.5 、在农药残留检测领域的应用
农药是农业发展的必需品,中国自古以来就是农业大国,农药使用量巨大。农药在提高农产品产量,保证人类粮食储备方面做出了巨大贡献。但同时由于大多数传统农药对人体会产生毒副作用,如果使用不当就会扩散到空气中,渗透到土壤和地下水中,再通过食物链进入人体,在人体内富集,当农药在人体内达到一定浓度时就会造成人体急性或慢性中毒,对人体危害极大。传统的农药残留检测方法多是靠色谱仪等大型仪器分析,这些仪器价格昂贵且使用起来耗时耗力,只能由专业人士在实验室进行检测,不适合大范围的普及推广。因此研发出方便快捷、准确安全的农药残留检测方法一直是农业领域的重中之重。BALA[20]等开发了一种基于未改性的金纳米粒子和有机聚电解质(PDDA)相互作用原理来检测溶液中农药添加剂马拉硫磷的新型传感器。当适体与PDDA结合时会抑制金纳米粒子团聚,溶液呈红色,而将适体特异性农药添加至溶液中时,适体与农药结合,金纳米粒子团聚,溶液呈蓝色。该检测方法简单快捷,有望投入实际应用中。WANG[21]等基于金纳米探针开发了双响应免疫层析方法检测氰戊菊酯。将鲁米诺还原的金纳米粒子标记到氰戊菊酯单克隆抗体上作为比色/化学发光探针,通过竞争模式,样品溶液中的氰戊菊酯与其相应的包被抗原竞争结合鲁米诺还原金纳米粒子标记的氰戊菊酯单克隆抗体,在竞争免疫反应结束后,捕获的双读数探针的颜色很容易被肉眼观察到,可作为定性的比色信号。随后,在测试线上触发鲁米诺-双氧水化学发光反应后,可将化学发光信号采集为定量信号。与利用两个不同的探针相比,具有双响应特性的单个探针操作更简单,成本更低,且弥补了传统试纸条灵敏度低、线性范围窄的缺点,为现场检测提供了新方法。
图2 基于鲁米诺还原纳米金粒子的双读数试纸条检测原理
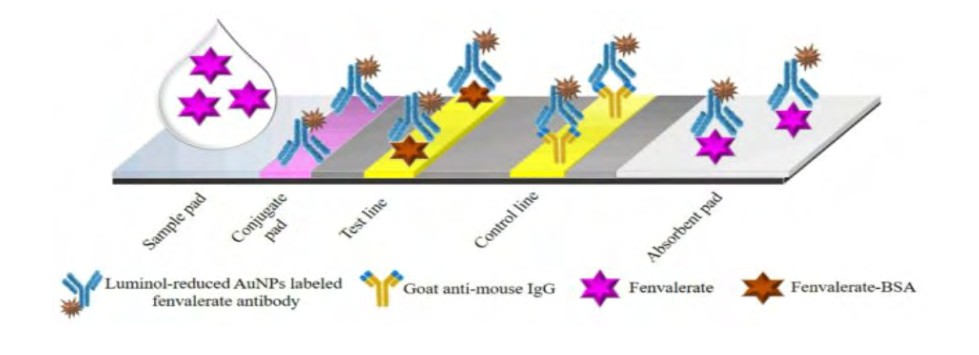
3.6 、在催化领域的应用
相比较传统催化剂,纳米催化剂的比表面积极大,表面的悬空键也更多,化学反应活性更强。块体的金对电催化反应显示惰性,但纳米级的金粒子由于很高的比表面积对许多反应具有高催化活性,且能够在常温甚至低温下进行催化。金纳米颗粒虽然有很强的催化活性,但却很少单独作为催化剂使用。一方面是因为成本较高,另一方面是因为在反应过程中超细粒径的金纳米粒子由于具有较高的表面能而容易聚集,导致其催化活性降低。因此人们常将金纳米颗粒负载在成本较低的固体载体上,例如碳材料、聚合物、磁性材料和金属氧化物等以形成复合纳米催化剂。这种做法被认为是减少纳米粒子聚集的有效策略,同时因金纳米粒子具有局域表面等离子体共振(LSPR)效应[22]和载体之间存在强烈的协同作用[23],还可以进一步提高其催化活性和稳定性。
甲醛属于一类致癌物质,却总是能悄无声息的潜伏到我们的身边。而处理甲醛污染最吸引人的方法是将其催化氧化为CO2和H2O,其去除效率高且没有二次污染。室温催化甲醛氧化的催化剂根据是否含有贵金属可分为两种[24]:贵金属催化剂和非贵金属氧化物。负载在其他材料上的贵金属通常比非贵金属氧化物催化剂具有更高的催化甲醛氧化活性,其中金纳米粒子由于良好的化学稳定性和环境友好性而备受关注。ROCHARD[25]等使用沉积-沉淀法将不同质量百分比的金纳米颗粒分散在Ce O2上,并通过煅烧Co结合Au/Ce O2基催化剂中。该催化剂中Co在直接与Ce3+量相关的氧空位形成中有益处,形成的氧空位在增强催化剂催化甲醛氧化的催化活性中有双重作用,Ce3+代表成核中心,用于稳定活性Au离子物质,同时稳定气态氧。在25℃下对负载不同金纳米量的催化剂进行比较,质量分数3%的金纳米催化剂显示出比其低金催化剂更高的甲醛转化率,在室温催化甲醛反应中表现优秀。QU[26]等利用模板方法来制备多孔金掺杂的铈和氧化钴(Au-Cex Coy)材料,得到大表面积纳米管有序阵列结构,具有高催化活性。而后再将Au-Cex Coy负载到氧化石墨烯(GO)表面,赋予催化剂能够再循环能力。催化剂在60℃时甲醛的转化率能达到100%,在消除甲醛方面有很好的应用前景。
CO是一种无色、无味的气体,可以与血红蛋白相结合,使其失去输氧能力,严重的甚至会威胁到人们的生命安全。而工业生产过程与日常生活中的天然气不完全燃烧、煤气泄漏等都可能会使CO排放到空气中去,稍不注意就会成为威胁人们身体健康的隐形杀手,因此在室温或低温下消除CO就具有重要的实际意义。JIN[27]等通过水热法制备直径分别为5、20 nm的二氧化铈,再经过沉积沉淀法将金纳米粒子负载在Ce O2载体上。经表征发现,Ce O2载体尺寸为20 nm催化剂(Au/Ce O2-20)表面被分散均匀的Au3+和Auδ+(0<δ<1)覆盖,而Ce O2载体尺寸为5 nm催化剂(Au/Ce O2-5)表面的主要物质是Au3+。Auδ+对CO具有更强的吸附作用,促进Au/Ce O2-20在CO氧化上有更好的催化活性。HAN[28]等用水热沉积沉淀法制备了新型的Au/α-Fe2O3类催化剂。该催化剂在30℃条件下运转60 h仍能完全转化CO,具有有效的低温CO氧化活性和优异的稳定性,有望用于工业CO排放控制。
4 、结束语
金纳米颗粒作为一种多功能材料具有广阔的应用前景。金纳米颗粒具有良好的电子学和物理学特性、表面易于修饰等优点,使得金纳米颗粒成为了学术研究领域中被研究最广泛的纳米材料之一。伴随其合成工艺的不断发展,相信不久的将来金纳米粒子的研究和应用开发会不断拓展到越来越多的领域。
参考文献
[1]HE H, XIE C, REN J.Nonbleaching fluorescence of gold nanoparticles and its applications in cancer cell imaging[J]. Analytical Chemistry,2008, 80(15):5951-5957.
[2]WHETTEN R L, KHOURY J T, ALVAREZ M M, et al. Nanocrystal gold molecules[J]. advanced materials, 1996, 8(5):428-433.
[3]TURKEVICH J, STEVENSON P C, HILLIER J. A study of the nucleation and growth processes in the synthesis of colloidal gold[J].Discussions of the Faraday Society, 1951, 11:56-75.
[4]JANA N R, GEARHEART L, MURPHY C J. Wet chemical synthesis of high aspect ratio cylindrical gold nanorods[J]. Journal of Physical Chemistry B, 2001, 105(19):4065-4067.
[5]BRUST M, WALKER M, BETHELL D, et al. Synthesis of thiolderivatised gold nanoparticles in a two-phase Liquid system[J].Chemical Communications, 1994(7):801.
[6] MARTIN C R. Nanomaterials:A membrane-based synthetic approach[J]. Science, 1995, 266(5193):1961-1966.
[7]YU Y Y,CHANG S S,LEE C L,et al. Gold Nanorods:electrochemical synthesis and optical properties[J]. Journal of Physical Chemistry B,1997, 101(34):6661-6664.
[8]谷伟,张锦岚,彭亮,等.不同尺寸、形状和组成的金纳米颗粒的光热特性:在癌症治疗中的应用[J].红外与激光工程,2018,47(11):386-394.
[9] ALI MOUSTAFA R K, AMINUR R M, WU Y, et al. Efficacy,long-term toxicity, and mechanistic studies of gold nanorods photothermal therapy of cancer in xenograft mice[J]. Proceedings of the National Academy of Sciences, 2017, 114(15):E3110-E3118.
[10]CHEN J, LIN L, YAN N, et al. Macrophages loaded CpG and GNR-PEI for combination of tumor photothermal therapy and immunotherapy[J]. Science China Materials, 2018, 61(11):1484-1494.
[11] GONG R D, CHEN G M. Preparation and application of functionalized nano drug carriers[J]. Elsevier B.V, 2016, 24(3):254-257.
[12]FENG Y, CHENG Y, CHANG Y, et al. Time-staggered delivery of erlotinib and doxorubicin by gold nanocages with two smart polymers for reprogrammable release and synergistic with photothermal therapy[J]. Biomaterials, 2019, 217:119327.
[13]GUO X M, LI W, ZHOU J L, et al. Specific photothermal ablation therapy of endometriosis by targeting delivery of gold nanospheres[J]. Small, 2017, 13(15):1603270.
[14]FENG Q S, SHEN Y J, FU Y J, et al. Self-assembly of gold nanoparticles shows microenvironment-mediated dynamic switching and enhanced brain tumor targeting[J]. Theranostics, 2017, 7(7):1875-1889.
[15]PENG C Q, YU M X, HSIEH J T, et al. Correlating anticancer drug delivery efficiency with vascular permeability of renal clearable versus non-renal clearable nanocarriers[J]. Angewandte Chemie,2019, 131(35):12204-12208.
[16]LU S, LI X, ZHANG J, et al. Dendrimer-stabilized gold nanoflowers embedded with ultrasmall iron oxide nanoparticles for multimode imaging-guided combination therapy of tumors[J]. Advanced Science,2018, 5(12).1801612
[17]TSVIRKUN, DARYA, BEN N, et al. CT imaging of enzymatic activity in cancer using covalent probes reveal a size-dependent pattern[J]. Journal of the American Chemical Society, 2018, 140(38):12010-12020.
[18]HUO S, JIANG Y, GUPTA A, et al. Fully zwitterionic nanoparticle antimicrobial agents through tuning of core size and ligand structure[J]. ACS Nano, 2016, 10(9):8732-8737.
[19]HU D, LI H, WANG B, et al. Surface-adaptive gold nanoparticles with effective adherence and enhanced photothermal ablation of methicillin-resistant staphylococcus aureus biofilm[J]. ACS Nano,2017, 11(9):9330-9339.
[20]BALA R, KUMAR M, BANSAL K, et al. Ultrasensitive aptamer biosensor for malathion detection based on cationic polymer and gold nanoparticles[J]. Pubmed, 2016, 85(15):445-449.
[21]WANG W W, OUYANG H.Luminol-reduced Au nanoparticles based dual-signal immunochromatographic test strip for pesticide residues[J]. Microchemical Journal, 2019, 149:104055
[22]LIU X, WAN Y L, JIANG T, et al.Plasmon-activated nanozymes with enhanced catalytic activity by near-infrared light irradiation[J].Chemical Communications, 2020, 56(12):1784-1787.
[23]BERTHET M, SONGIS O, TAILLIER C, et al.Catalytic alkynylation of cyclic acetals and ketals enabled by synergistic gold(i)/trimethylsilyl catalysis[J]. Journal of Organic Chemistry,2017, 82(18):9916-9922.
[24]GUO J, LIN C, JIANG C, et al. Review on noble metal-based catalysts for formaldehyde oxidation at room temperature[J]. Applied Surface Science, 2018, 475:237-255.
[25] GUILLAUME R, GIRAUDON J M, FRANCESCA L L, et al. Au/Co promoted CeO2 catalysts for formaldehyde total oxidation at ambient temperature:role of oxygen vacancies[J]. Catalysis Science&Technology, 2019, 9(12):3203-3213.
[26]QU J, CHEN D, LI N, et al. 3D gold-modified cerium and cobalt oxide catalyst on a graphene aerogel for highly efficient catalytic formaldehyde oxidation[J]. Small, 2018(2):1804415.
[27]JIN Z, SONG Y Y, FU X P, et al. Nanoceria supported gold catalysts for CO oxidation[J].Chinese Journal of Chemistry,2018, 36(7):639-643.
[28]HAN Q, ZHANG D, GUO J, et al.Improved catalytic performance of Au/α-Fe2O3-like-worm catalyst for low temperature CO oxidation[J].Nanomaterials, 2019, 9(8):1118.





