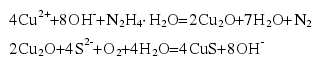第 4 章 基于石墨烯/硫化铜空心球过氧化氢电化学传感器
4.1 引言
石墨烯是一种由 sp2杂化的碳原子构成的片状碳纳米材料[68],具有蜂窝状的晶格结构[69]、大的比表面积[70,71]、良好的导热[39]和导电性能[72]、高的机械强度[73]等优点,在许多领域引起了广泛关注,如催化剂[74,75]、能量存储[76]、传感器[77,78,121]等。制备石墨烯的方法主要有机械剥落石墨法[122]化学气相沉积法[123]和还原氧化石墨烯法[124]等。还原氧化石墨烯法制备石墨烯的方法包括在真空或者惰性气体氛围内高温煅烧氧化石墨烯、在溶液中化学还原氧化石墨烯和电化学还原氧化石墨烯[125].
空心球纳米结构由于其特有的性能引起了广泛的关注,且被应用于很多领域,如药物运载[126]、催化剂[127]、传感器[128]、人造细胞[129]等。构建空心纳米结构的方法近几年有不少报道,主要有硬模板法、软模板法、Kirkendall 效应或 Ostwald 熟化引发的物理/化学自我转化过程等[130-133].硫化铜作为一种重要的半导体材料,具有独特的电子、光学、化学性能,在传感器[134]、催化剂[135]、太阳能电池[136]等方面具有潜在的应用价值。
本文以 Cu2O 纳米球为牺牲模板快速合成硫化铜空心球(CuSHNs),运用电化学法还原氧化石墨烯,构建石墨烯/硫化铜空心球过氧化氢(H2O2)电化学传感器,石墨烯与硫化铜空心球具有良好的协同作用,能够产生较大的响应电流信号,该检测方法具有制作方法简单、灵敏度高、选择性好等优点。
4.2 实验部分
4.2.1 仪器和试剂
透射电子显微镜(TEM)分析采用美国 FEI公司 Titan G2 60-300 显微镜;扫描电子显微镜(SEM,日本JEOL 公司 JSM-6610LV型);CHI660D 电化学工作站(上海辰华仪器有限公司);玻碳电极(GCE,天津艾达恒晟科技发展有限公司);铂电极(上海仪电科学仪器股份有限公司);饱和甘汞电极(SCE,上海仪电科学仪器股份有限公司)。
石墨粉、硝酸钠(NaNO3)、高锰酸钾(KMnO4)、三水合硝酸铜(Cu(NO3)2·3H2O)、九水合硫化钠(Na2S·9H2O)、聚乙烯吡咯烷酮(PVP)、氯化钾(KCl)、十二水合磷酸氢二钠(Na2HPO4·12H2O)、二水合磷酸二氢钠(NaH2PO4·2H2O)、过氧化氢(30%,V/V)、抗坏血酸(AA)均购自国药集团化学试剂有限公司;多巴胺(DA)购自于阿拉丁试剂(上海)有限公司;浓硫酸、盐酸、硝酸均购自株洲市星空化玻有限责任公司;N2饱和的 0.1 M 磷酸缓冲液(PBS,pH=7.0)为支持电解质溶液。实验室所用化学试剂均为分析纯,实验所用水为超纯水(电阻率为18.25 MΩ·cm)。
4.2.2 实验方法
4.2.2.1 氧化石墨烯的制备
在实验之前,所有玻璃仪器用王水(HCl:HNO3,3:1,V/V)浸泡 12 个小时,用超纯水清洗干净。氧化石墨烯的制备采用改进的 Hummers 法[88]:取 0.5 g 石墨粉和0.5 g 硝酸钠加入到装有23 mL 浓硫酸的三颈烧瓶中,在冰水浴中搅拌混合 5 min,缓慢加入3 gKMnO4,剧烈搅拌 10 min,然后在35 ℃下水浴加热1 h,形成稠密糊状后加入40 mL超纯水,把温度升高到95 ℃,加热30 min,之后再加入 100 mL 超纯水,把温度降低至50 ℃,然后再缓慢滴加 3 mL H2O2(30%,V/V),溶液的颜色由深棕色变成黄色,把所得的物质先进行低速离心2 min (1000 rpm),重复3 次,直到沉淀中所有可见异物去除,留取上清液。然后高速离心15 min (8000 rpm),重复 2 次,去除小的氧化石墨烯片和水溶性副产物,所得沉淀用100 mL10% 盐酸溶液清洗,接着用超纯水洗至中性,最后把所得沉淀进行真空干燥,即得氧化石墨烯(GO)。用电子天平秤取5 mg GO,加入到10 mL超纯水中,经过超声,使得 GO 全部剥落成单片,所得溶液为 0.5 mg/mL 的 GO 溶液。
4.2.2.2 硫化铜空心球的制备硫化铜空心球的制备方法是对 Zhu 等人[137]报道的方法进行了修改。在室温下将100μL 0.5 M Cu(NO3)2加入到25 mL 含有0.24 g PVP 的水溶液中,磁力搅拌均匀。然后向上述混合液中缓慢加入25 mL(pH=9.0)的 NaOH 溶液,随后加入 8 μL 水合肼,磁力搅拌5 min.将 200 μL 的 Na2S 溶液(320 mg/mL)加入到上述溶液中,在温度为 60 ℃水浴下反应 2 h.最后将所得产物离心(8000 rpm,10 min),用去离子水和无水乙醇清洗所得离心物,将离心所得沉淀分散在超纯水中。
4.2.2.3 石墨烯/硫化铜空心球修饰电极的制备(传感器的构建)玻碳电极经 0.05 ?m 氧化铝粉抛光后,用超纯水和无水乙醇超声清洗干净。在玻碳电极表面滴加一定量 0.5 mg/mL 氧化石墨烯,在室温下自然干燥,然后在 0.5 M NaCl溶液(pH=7.0)中,于-1.3 V电位下进行电化学还原300s,得到石墨烯修饰电极[89,90],然后滴加一定量硫化铜空心球溶液,自然干燥,备用。传感器的构建过程及反应机理,如图 4.1 所示.
4.2.2.4 电化学测量
采用三电极体系,石墨烯/硫化铜空心球修饰的玻碳电极为工作电极,以饱和甘汞电极(SCE)为参比电极,铂片电极为对电极。选用计时电流法在不断搅拌的 N2饱和的0.1 MPBS 中进行电化学测量。
4.3 结果与讨论
4.3.1 石墨烯、氧化亚铜模板和硫化铜空心球的形态表征
图 4.2A 为石墨烯修饰电极的扫描电镜图。从图中可以看到石墨烯呈薄片状结构,表面有很多不平的皱褶,与文献报道类似[91].图 4.2B 为氧化亚铜纳米球扫描电镜图。
从图中可以看出,氧化亚铜纳米球呈规则的球体结构,平均直径约为130 nm.
图 4.2C 和图 4.2D 为不同放大倍数的硫化铜空心球的透射电镜图,如图所示,所合成的硫化铜空心球形状规则、尺寸大小较为均匀,平均外径约为 150 nm,外壳的平均厚度约为 25 nm.硫化铜空心球的形成机理与 Zhu 等人[137]所发现的机理类似,形成机理如图 4.3 所示。
氧化亚铜纳米球为牺牲模板,在 60 ℃母液中发生硫化作用,形成这种空心结构。
简言之,就是以氧化亚铜纳米球为牺牲模板,加入 Na2S 后,电离出的 S2-与氧化亚铜发生硫化作用,在氧化亚铜表面形成硫化铜纳米颗粒,随着反应时间的增加,生成的硫化铜纳米颗粒聚集形成壳状空心结构。最终氧化亚铜反应完全,硫化铜空心壳状结构取代了最初的氧化亚铜纳米球,形成硫化铜空心球。反应方程式如下所示[137]:
4.3.2 传感器的电化学性能
4.3.2.1 电极的电化学表征
图 4.4 为氧化石墨烯修饰电极(a)、裸玻碳电极(b)、石墨烯修饰电极(c)在 0.1 MK3[Fe(CN)6]/K4[Fe(CN)6] (含 0.1 M KCl)中的循环伏安图。从图中可知,氧化石墨烯修饰电极(a)相比于裸玻电极(b),没有明显的氧化还原峰,这是由于氧化石墨烯导电性能差,严重阻碍了电子传递。然而,氧化石墨烯在-1.3 V下还原成石墨烯,氧化还原峰显着增大,这是因为石墨烯具有良好的电催化活性及导电性,促进了电化学探针[Fe(CN)6]3-/4-和电极表面之间的电子传递。
图 4.5 为裸玻碳电极(a)、石墨烯电极(b)、石墨烯/硫化铜空心球电极(c)在 N2饱和的 0.1 MPBS (pH=7.0)溶液中的循环伏安图。从图中可知,石墨烯修饰电极(b)比裸玻碳电极(a)具有更大的电流响应信号,这是因为石墨烯具有良好的电催化活性及导电性,因此,石墨烯可以明显改善玻碳电极电化学性能。石墨烯/硫化铜空心球修饰电极相比于裸玻碳电极和石墨烯修饰电极,在-0.26 V 和-0.10 V 出现一对氧化还原峰,这都归因于Cu2S/CuS 氧化还原电子对[138].
图 4.6 为石墨烯/硫化铜空心球修饰电极在 N2饱和的 PBS (pH=7.0)的循环伏安图,图中 a 为缓冲液中无过氧化氢存在的循环伏安图,出现了一对氧化还原峰,这归因于Cu2S/CuS 氧化还原电子对[138].图中 b 为加入 1 mM 过氧化氢后的循环伏安图,由图可知,加入过氧化氢后,如图所示还原峰显着增大,氧化峰明显减小,结果表明石墨烯/硫化铜空心球修饰电极对 H2O2具有良好的电催化还原活性。
图 4.7 为石墨烯/硫化铜纳米球(a),硫化铜空心球(b),石墨烯(c)修饰电极在-100 mV电位下于0.1 M PBS 中连续加入 2 mM H2O2的计时电流响应图。石墨烯/硫化铜空心球修饰电极的响应电流最大(11.2 ?A),是硫化铜空心球修饰电极响应电流(3.8 ?A)的 2.95倍,是石墨烯修饰电极响应(2.4 ?A)的 4.7 倍。石墨烯/硫化铜空心球修饰电极响应电流值大于硫化铜空心球修饰电极与石墨烯修饰电极的响应电流之和,表明石墨烯/硫化铜空心球电极增强的电流信号不仅由电活性表面积的增大引起,还在于石墨烯与硫化铜空心球具有良好的协同作用,显着提高了传感器对 H2O2的电催化活性。
4.3.2.2 实验条件优化
图 4.8A 为石墨烯用量对 H2O2电化学信号的影响。由图可知 H2O2响应电信号随着石墨烯用量的增加而增大,在 8 ?L 处达到最大值,继续增加石墨烯用量,响应电流值反而减小,这可能是电极表面形成的石墨烯薄膜厚度过大,阻碍了电子传递。因此,石墨烯的优化用量为 8 ?L.图 4.8B 为氧化石墨烯还原时间对 H2O2响应电流信号的影响。
由图可知,随着还原时间的增加,响应电流值在初始阶段增加缓慢,240 s 后急剧上升,并于300 s时基本趋于稳定。这是因为还原时间达到300 s时氧化石墨烯已基本还原完全,继续延长还原时间响应电信号没有显着改变。所以最佳还原时间为 300 s.图 4.8C 为硫化铜空心球用量对 H2O2响应电流值的影响。由图可知,在 2-15 ?L 范围内,随滴加量的增大,传感器对 H2O2的响应电流信号先增大后减小。当滴加量为 5 ?L 时,测出的响应电流值最大。因此取 5 ?L 为硫化铜空心球的优化用量。图 4.8D 为缓冲溶液 PBS 的pH 值对过氧化氢电信号的影响。如图所示,pH 值在 6.0-7.0 范围之内变化时,H2O2的响应电流值逐渐增加,当 pH 等于 7.0 时,响应电流值达到最大。继续增大缓冲液 pH 值,H2O2响应电流值逐渐减小。因此选用 pH 为 7.0 的 PBS 为支持电解质溶液。图 4.8E 为工作电位对 H2O2响应电流信号的影响。选取工作电位在-500 mV到 500 mV范围内,对H2O2响应电流信号进行考查。从图中可以看出,随着电位的不断负移修饰电极对 H2O2的响应信号逐渐增大,当电位到达-300 mV时响应达到最大值,继续负移信号逐渐减小。向正方向增加工作电位,响应电流值增加缓慢。因此,取-300 mV为优化工作电位。
4.3.3 传感器的分析性能
4.3.3.1 线性实验
图 4.9 为石墨烯/硫化铜空心球修饰电极在优化条件下的 H2O2标准曲线图,响应电流 值 与 H2O2浓 度 在 0.005-4.0 mM 范 围内 呈 良 好的 线 性 关系 , 线性 方 程y=7.1773x+0.3276,相关系数 R=0.9989,检测下限为 3.0 ?M.所研制的 H2O2传感器与其他报道传感器分析性能相比较,如表 4.1 所示。相比于文献[138-147]报道的传感器,我们研制的 H2O2传感器具有较宽的线性范围和较低的检出限。这都归因于石墨烯与硫化铜空心球具有良好的协同作用,显着提高了传感器对 H2O2的电催化活性。
4.3.3.2 干扰实验
如图 7 所示,加入相同量的过氧化氢、多巴胺和抗坏血酸,结果发现 DA(0.44 μA)和 AA(0.25 μA)响应电信号远小于 H2O2(9.7 μA)响应电信号,由此可以得出 DA 和 AA对石墨烯/硫化铜空心球修饰电极测定 H2O2干扰较小,说明我们所研制的传感器具有良好的选择性及抗干扰能力。
4.3.3.3 重复性及重现性实验用同一支修饰电极测定2 mM H2O2,连续测6 次,相对标准偏差(RSD)为2.27%,表明传感器能够重复使用。取 6 根修饰电极测定 2 mM H2O2,考察传感器的重现性,相对标准偏差(RSD)为2.46%,表明传感器的重现性较好。
4.4 小结
本文采用计时电流法建立了石墨烯/硫化铜空心球修饰电极快速测定 H2O2的方法。
我们采用电化学法绿色制备石墨烯,以 Cu2O 纳米球为牺牲模板合成硫化铜空心球。由于石墨烯具有大的比表面积和良好的导电性等优点,且能够与硫化铜空心球产生良好的协同作用,显着提高了传感器对 H2O2的电催化活性。所研制的传感器具有制作方法简单、灵敏度高、选择性好、线性范围宽(0.005-4.0 mM)、检测下限低(3.0 ?M)等优点,为石墨烯复合材料制备传感器提供了一种新的方法。