��������ʳƷ�������ѧ�����IJ��Ϸ�չ���������\�������ʳƷ�IJ������ֵ��ռʳƷ�������ҵ����Ҫ��λ��ʳƷ�����������Ի������顢���ӿ�¡�ȼ���Ϊ�����������ﷴӦ���̡��������ʵķ��봿���ȼ���Ϊ�ص�Ĺ�ҵ�����̻������������壨�������壩����������Ҫ��ʳƷ��Ӧ�ü�����������ʳƷ���\������8ƪ������ҽ���ο���
ʳƷ���\�����ĵ�һƪ��PR������ũ��Ʒ��ȫ����е�Ӧ��
����ժҪ����������ӹ�����Ϊ�������ڹ��ڷ�չ������һ�ּ�⼼��,�߱������Ʒ�����١������ȸߡ�����ٶȿ���ŵ�,�ѱ����ڻ�����⡢ҽ����ϡ�ҩ��ɸѡ����������ѧ��������ѧ������������ż����ķ�չ,���ѧ�߽��������\���������,�ڴ���оƬ�������β�ͬ�������Կ�ԭ���弰�źŷŴ�����,����������ӹ���������Ӧ�õ�ũ��Ʒ��ȫ�ļ���С�ͨ�����ܸü�����ũ��Ʒ��ũ��ҩ�С����R�������ʳƷ���Ӽ����ؽ�����ת�������Ӧ�����,����ʹ���������˽��������ӹ�������ʳƷ��ȫ���ķ�չ��״,Ϊ���ڸ�����Ľ�һ����չ�ṩ���Խ�������ϡ�
�����ؼ��ʣ���������ӹ���; ���ﴫ��; ũ��Ʒ��ȫ; ���; Ӧ��;
����Applications of SPR Biosensing Technology in Agricultural Products Safety Detection
����Wang Tingting Hu Jiandong
����Henan Nongda Xunjie Measurement Technology Co., Ltd Department of Electrical Engineering, Henan Agricultural University
����Abstract��Surface plasmon resonance(SPR) as a novel technology has advantages of small sample volumes,high sensitivity and fast detection speed, which is widely applied in environmental detection, medical diagnosis, drug screening, proteomics, genomics and many other fields. With its development, SPR is combined with biotechnology, then modified by specific antigen, antibody and signal amplification factor, and widely used in safety detection of agricultural products. The paper introduces the application of SPR in detection of pesticide and medicine residues, animal disease, microbe, food additives, heavy metal and transgenic test in agricultural products. The study could provide certain references for understanding the development status of SPR in food safety test.
����0 ����
��������21����������“�����”��“������”�ȶ�ζ���ʳƷ��ȫ�¼��ķ�������ʹ�������Ⱥ��Խ��Խ��ע������ȫ�����ɴ˳�Ϊȫ����ע�Ľ��㡣2014����������ʳƷҩƷ����ܾ֣�ũҵ����ʵ***�����“�ĸ�����”Ҫ��չ��ȫ��ʳƷ��ȫʾ�����д�����ũ��Ʒ������ȫ�ش�����“˫��˫��”����Ӵ��г���ܣ���Դͷ�ž�����ȫ���ء�2017����ļ��ȹ���ʳƷҩƷ�ල�����ܾ�ʳƷ��ȫ��飬���ϸ���Ʒ23766���Σ�ռ������������2.2%�����У�ʳƷ�г���Χ��������ʹ��ʳƷ���Ӽ�����ռ���ϸ�������27.7%��ʳƷ��ũ��ҩ����ָ�겻�ϸ�����ռ���ϸ�������25.1%��ʳƷ��������Ⱦ����ռ���ϸ�������24.4%��ʳƷ���ؽ�����Ԫ����Ⱦ����ռ���ϸ�������3.3%��ʳƷ�����ﶾ����Ⱦ����ռ���ϸ�������1.2%������֮������ﶾ�ء�����ָ��IJ��ϸ���β��ܳԵķ��ģ��Եð���?����Ҫ��Դͷץ��ʳƷ�İ�ȫ�Լ��Ҳ�DZز����ٵ��ֶ�֮һ��Ŀǰ����ũ��Ʒ��ȫ���ļ�����Ҫ�й�����[1]��ɫ����[2,3,4]�����\��[5]�Լ���������[6]�ȷ���������ѧ��������ӹ���(Surface Plasmon Resonance,SPR)�����״α�����20���ͳ�������Ϊһ�ּ�ⷽ���������ڼ������CO2��O2��Ũ��[7]�����Ÿü����IJ��Ϸ�չ�����������\����ϣ��γ�SPR���ﴫ���������Լ�����еľ��������Է�Ӧ��������ӡ���ˣ�SPR����Խ��Խչʾ������Ҫ��Ӧ�ü�ֵ����Խ��Խ��IJ��뵽ũ��Ʒ��ȫ�Ե����۹�����[8,9]��
����1 SPRԭ��������
������������ӹ�����Ϊһ��������ѧ�������������1902��[10]�������ԭ���ǵ�һ��Pƫ�����һ���Ƕ����䵽�⾵���棬�ڽ�Ĥ����ʽ��������������Ӳ���������Ⲩ��������ˮƽ�����ͱ��������������������ʱ���ͻ���������������г����ʱ�����������������ת�Ƶ�������������ϣ�ʹ��Ӧ�ķ�����ǿ����������ͼ1����1983��Liedberg��[11]���ñ�������ӹ������о���ԭ����֮�������ã��״ν�SPR����Ӧ�������ﻯѧ��⡣����SPR������������ŵ㣬������Ʒ�����١������ȸߡ�����ٶȿ죬�ѱ��㷺���ڻ������[12]��ҽ�����[13]��ҩ��ɸѡ[14]����������ѧ[15]��������ѧ[16]����������Ľ�ϵͳ����SPR������ũ��Ʒ��ȫ����Ӧ����״������Ϊ���ϲ�����ȫ�ṩһ���µ�˼·��
����2 SPR������ũ��Ʒ��ȫ����е�Ӧ��
����2.1 SPR������ũ��Ʒ��ũ��ҩ�м���е�Ӧ��
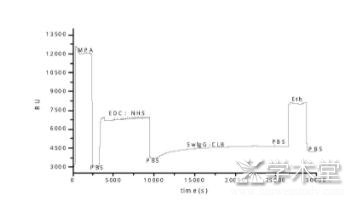
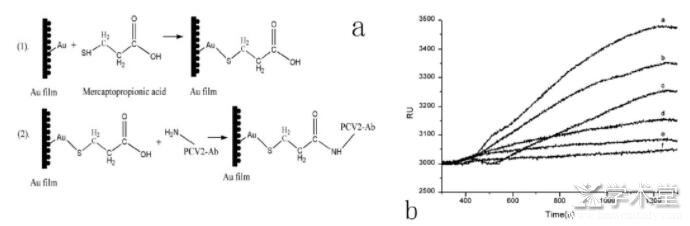
����ũ��Ʒ�е�ũҩ������Ҫָ�����ء�ɱ����ࡢ�����ٽ����ȡ�����ʹ�ú���ũҩ������ũ��Ʒ�����彡������������в���ÿ�����Ϊʶ����ӣ����ũҩ��Ŀǰ������Ӧ����㡢���ձ�ļ�ⷽ�������ſƼ��ķ�չ����ԭ����������Խ��ͨ��SPR����Խ��Խ�㷺��Ӧ�õ�ҩ������ļ�⣬�����������Ͻ��ͣ���ⷶΧ��������Hu[17]���������������ͨ����ѧ�����̶��ڴ��н�Ĥ���棬�������������������ԭ����ԭ���������Խ�ϣ������Ĥ�������ʵ����ı仯�������ʵĸı䣬ͨ��������Ӧֵ(response unit,RU)�ı仯ȷ����Һ�������������Ũ�ȣ�ͼ2�����о�������������������ı����ߣ������Ϊ1.26 ng/mL��ʯ�õ�[18]���ݿ�ԭ���巴Ӧ��ͨ������װ�ڽ�Ĥ����̶�������ӣ����ڼ�ⲻͬ����Ũ�ȵİ�����ù�أ���ͷֱ�Ũ��Ϊ1.25 ng/mL��ͬʱ��������Ʒ���١��¶ȡ�pHֵ������Ũ�ȶԼ������Ӱ�졣
����
����ͼ1 SPR���ԭ��
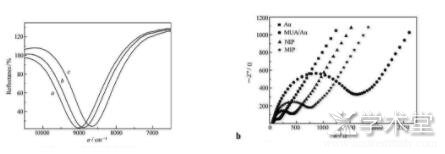
�������ŵ绯ѧ����������ӡ������(Molecular imprinted polymers,MIP)�ķ�չ��1998�꣬Lai��[19]�Ʊ����������ʺͿ���MIP-SPR�����������״ν������ʼ����������������MIP-SPR�����������������������ʵ������Խ�ϣ������Ϊ0.4 mg/mL���Դˣ�MIP-SPR������ũҩ����ҩ�����ﶾ�ص������Ӧ��ȡ���˽Ϻ÷�չ��2016�꣬Shrivastav��[20]�������ڶ�ģ�����ϣ�Ȼ������Ĥ����Ϳ������ڱ����ķ���ӡ���ۺ���Ʊ���һ�����͵Ļ��ڹ���ά���������ӡ���ۺ����SPR���ﴫ������������������ʱ���������ӡ���ۺ����ϣ��������������ʸı䣬SPR���Կ���ȷ�IJ������ֱ仯�������ֲ�ͬŨ�ȵİб����ʡ�����֤�ô������Ա����ļ����LODֵ�ɴﵽ2.5×10-6μg/L����ⷶΧΪ10-4��10-1μg/L��Zhang��[21]�Ʊ��Ŀ���ù�ط���ӡ��SPR���������Կ���ù�ص����Լ�ⷶΧΪ1.0×10-7��1.0×10-8moL/L���Է����п���ù�صļ���ﵽ1.20×10-8moL/L��
����SPR�����������������Ĥ�����������ı仯��������ʵģ����������е�ũҩ����С�������ʣ�ֱ�Ӽ����������������仯�����ԣ�������SPR������ũҩ��������е�Ӧ�á�������������ѧ��ͨ���źŷŴ�ʵ�ּ��С��������[22,23,24]���������ʵļ�ⷶΧ��Bianco M���ض����е�˫��DNA�����徭�ϻ����κ�ͨ������װ����Ĥ��ʽ�̶��ڴ��н�Ĥ���棬���ڼ�������л������ù���أ������Ϊ0.005 ng/mL[25]��Wang��[26]����BiacoreT200�����ѱ���������ص�CM5оƬ����ͨ����DNA���ṹ���������϶���̻��Ļ��ؿ���������(Apt76)�������SPR���崫������оƬ�����ȼ������ԡ�ʵ���У��������Ļ��ؼ��Ļ�����Ϊ80.20%��114.3%����ͼ����Ϊ0.0069μg/kg��
��
����ͼ2 SPR����������������Ӧ����[17]
����2.2 SPR�����ڶ��R�����������е�Ӧ��
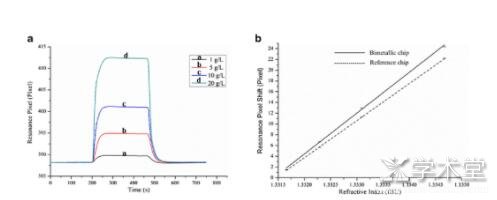
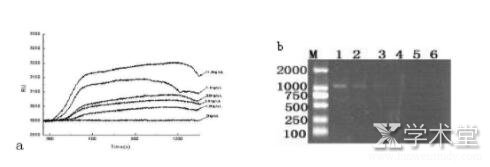
������ͳ�Ķ����߲���ⷽ���������к�ʱ�������ȵ͡������Ը��Լ����ܸ��ŵ�ȱ�㣬�������ڴ�Χ����ȷ�ؼ��ﲡ��[27]��SPR���ﴫ�����ķ�չΪSPR����Ӧ���ڶ��R������ṩ���Ⱦ�������2012�꣬Hu[28]������������Ƶ�SPR�������ϵͳ���״ζԼ������Ҳ������м�⣬ͨ������ϡ�ͣ���ϡ�ͱ�����RU��Ӧֵ���ϵ���ﵽ0.97982��ͬһϡ�ͱ���������������ԣ���Ա�ƫ��(RSD)Ϊ3.6%����ͼ����Ϊ2.5 ng/mL��2014��Hu[29]ͨ������װ����Ĥ�ֶ���Բ��������(Porcine circovirus��PCV2)�ͽ��м�⣨ͼ3��������ﵽ0.04 mg/mL��ͨ����Ʒ���ӽ��л��������飬�����ʷ�ΧΪ81.0%��89.3%��
�����й�ÿ����ʳ�ú����²�����ũ��Ʒ�������ʳ���ж��¼�ռ������30%��90%������SPR������ϸ��������ļ������귢չ�Ͽ죬������Ҳ���̵õ�ͻ�ơ�2013��Wang���������������ԭ����O157H7����Ч�ر�������ϸ����������������Ч��ⷶΧ��ȱ������˶Դ˾�����������[30]��Naboka��[31]��ȫ�ڷ�����Բ��ȷ�(total internal reflection ellipsometry,TIRE)��LSPR���ã��˷���LSPR����ʧ��˥�����ȵ�ȱ�㣬��ù�����صļ����������ߵ�0.1 ng/mL��
����2.3 SPR������ũ��Ʒ���Ӽ�����е�Ӧ��
����ʳƷ���Ӽ��ĵ���һ������ٽ���ʳƷ��ҵ�ķ�չ��������Ϊ�ִ�ʳƷ��ҵ����꣬�����ͬʱ����һЩ�����̼ҵķǷ���������ӣ���ʹ��ʳƷ���Ӽ������ʳƷ��ȫ���ⱻƵƵ������ʳƷ���Ӽ��ļ�ⷽ��������Ҳ�ڲ��������еõ��Ͽ췢չ����������ӹ���������������ȵ����ܱ���ϲ�����ܴ����[32]ͨ�����������ۺϼ�����SPR����оƬ����̶�һ���յ����ӡ������Ĥ�����ڼ�������ۺ�����Ʒ�е��յ������ͼ4���������ֱ�Ϊ3.4×10-10moL/L��2.5×10-10moL/L����������[33]�����ĸ���Ҷ-��������ӹ��������ڼ�����ʻƣ������13μg/L���о����������Ƚ����ʻ���ţѪ�嵰����ϣ�Ȼ��ż����ͨ�����������̶���SPR���н�Ĥ���棬���ʱ�ֽ����ʻ���Һ�����ʻ�-С��¡�����ϣ���Ӧ��ֺ���ӦҺ�����Ʊ��õ�оƬ��оƬ�Ϲ̶������ʻ�-ţѪ�嵰�ͻᲶ�������δ��Ӧ�����ʻ�-С��¡���壬ͨ��������ʵ�ּ�����ʻơ�
��
����ͼ3 a�����Բ���������͵�����װ����ʶ��Ĥ��b��ͬŨ�Ȳ����ļ����Ӧ����[29]
����a��g��PCV2Ũ�ȷֱ�Ϊ10.0��7.5��5.0��2.5��1.0��0.5 mg/m L
����2.4 SPR�������ؽ�������е�Ӧ��
���������ؽ�����Ⱦ�¼��ż����ʣ��Ӻ��϶�ͯѪǦ�����¼������ؽ�����Ⱦ“������”�ȵȣ��ɼ��ؽ�����Ⱦ��Ӱ�쵽���ǵĽ�������ؽ�����ָ�ܶȴ���4.5 g/cm3�Ľ�������������As��Hg��Pb��Cd��Gr��Ag��Ni��Cu��Au�ȹ���45�֡����ũ��Ʒ���ؽ����ļ�⼼��ˮƽ�����ũ��Ʒ���ؽ����������⣬�Լ�ǿũ��Ʒԭ���ϼ���Ʒ��Ⱦ�ļ�ؾ�����Ҫ���塣������ѧ���ڲ����������м�ⷽ��ͬʱ��Ҳ�������µļ�����Pang��[34]ͨ�����ƵĽ�������Ĥ-SPR�����ؽ���������(Cd2+)�ļ�⡣�����ڲ����϶���2 nm��ȵĸ�(Cr)����Ϊ𤸽�㣬Ȼ������һ��40 nm�����Ĥ�������10 nm�Ľ�Ĥ����ɸ���Ĥ�Ʊ���Ȼ��ţѪ�嵰��(BSA)ֱ�������ڽ�Ĥ���棬���ڼ��Cd2+�������Ըý�������Ĥ-SPR��ͼ��ֵΪ0.01μM����ͼ5����Pelossof��[35]�����ȸ���Ѫ���ؼ�����DNAø��Pb2+���SPR�������ȣ���Pb2+�ļ���ֱ�Ϊ1×10-12moL/L��5×10-15moL/L��
����ͼ4 a��������ۺ�����Ʒ�е��յ�����SPR����оƬ����ͼ��b��������ۺ�����Ʒ�е��յ�����Au��NIP��MIP��MUA/Au���迹ͼ��[32]
����2.5 SPR������ת����ũ��Ʒ����е�Ӧ��
����������ת�����Ʒ��������ʳƷ��ȫ�ķ���˼⣬����μ��ת����ʳƷҲ��Ϊ��������߹��ĵ��ȵ㡣Ŀǰ�����ת����ļ����Ҫ�л��ڵ����ʵļ�ⷽ���ͻ���DNA�ļ�⼼�����֡�����SPR��������ת����Ƭ�ε��о����������2009��Ф�ر�[36]�����ϻ�ͷ��35S�����ӹѾۺ�����̽�����ε��ƽ��BiacoreоƬ���棬����������е�ת����PCR����Ƭ�Ρ�2013�꣬�����õ�[37]����SPR�������С���е�һ��ת�������У���PCR��Ӿ���ֵ��1�����Ҽ����Ϊ0.27 mg/L��ͼ6��������SPR�����Ի���Ƭ��ת¼�������о��IJ������룬ҲΪת����ʳƷ�ļ���ṩ��һ��˼·��
��
����ͼ5 a��ͬŨ�ȵ��Ȼ�����Һ�ڽ�������Ĥ�Ĵ���ͼ��b��ⲻͬ�����ʵ��Ȼ�����Һ�ļ�������[34]
��
����ͼ6 a��ͬŨ��ת����Ƭ�ε�SPR��Ӧ���ߣ�b��ͬŨ��ת����Ƭ�ε�PCR��Ӿ���[37]
����M.DNA marker;1��5��Ʒ����Ũ�ȷֱ�Ϊ11.5��7.1��3.9��1.9��1.5 mg/L;6.�հ���
����3 ����
����SPR������Ϊһ�ּ���ֶΣ��������ڹ����ⷢչ�������ݱ�������ϲ����ھ�SPR�������ڼ���ϵ������ȼ�����ޣ�������SPR��Ӧ������������ҽ�ơ������������ʼ�������ѧ��ʳƷ��ȫ�ȡ�������Ҳ���ɻرܵ���SPR����Ҳ��������ȱ�ݡ�����С���ӵ��������д���ߡ��豸����ȡ�����SPR��������������������Ҳ��Ӧ�˶�������LSPR[38]������ӡ��SPR[19,20,21]���绯ѧSPR[39]���Ź�SPR[40]�����Ӿ������SPR[41]��SERS-SPR����������[42]�ȵȡ�������һ�����IJ��Ϸ�չ��Ϊ����ʳƷ��ȫ����ϵ�Ӧ���ṩ��Ϊ������������
���������
����[1]��ϼ,�ɷ�,Ӧ���.���������������Ʒ����е�Ӧ�ú��о���չ[J].����ѧ�������,2009,29(7):1876-1880.
����[2]����ũ.���������������ɫ�̶���Ľ�չ[J].����������,2013,32(5):111-124.
����[3]Wang Q J, Yi R H, Mo C H. Determination of Quinolone Antibiotics in Water Using Solid Phase Extraction-High Performance Liquid Chromatography-Fluorescence Method[J].Animal Husbandry and Feed Science,2011,3(2):45-48.
����[4]Choma I, Grenda D, Malinowska I, et al. Determination of flumequine and doxycycline in milk by a simple thin-layer chromatographic method[J].JChromatogr B,1999,734(1):7-14.
����[5]����,������,��ΰ,��.������-���طŴ�ø�������������ⶨ���һ����������л���ũҩ[J].������ѧ,2011,39(3):346-350.
����[6]����.ʳƷ��Ⱦ���⼼���о���չ��ʳƷ��ȫ��ⷽ�����о�[J].�й�ʳ����Ӫ��,2005,3:31-33.
����[7]Homola J, Yee S S, Gauglitz G. Surface plasmon resonance sensors:review[J].Sensors and Actuators B:Chemical,1999,54(1-2):3-15.
����[8]Rasooly A. Surface Plasmon Resonance Analysis of Staphylococcal Enterotoxin B in Food[J].Journal of Food Protection,2001,64(1):37-43.
����[9]Mifumi S, Yoko N, Zhang W, et al. Simple and rapid detection method using surface plasmon resonance for dioxins,polychlorinated biphenylx and atrazine[J].Analytica Chimica Acta,2001,434(2):223-230.
����[10]����ΰ,���.����������干�����ﴫ�������о���״[J].����������,2001,7(5):8-12.
����[11]Liedberg B, Nylander C, Lundstrom I. Surface plasmon resonance or gas detectlon and biosensing[J].Sensors&Actuators,1983,4:299-304.
����[12]Inamori K, Kyo M, Nishiya Y, et al. Detection and quantification of on-chip phosphorylated peptides by surface plasmon resonance imaging techniques using a phosphate capture molecule[J].Analytical Chemistry,2005,77(13):3979-3985.
����[13]Chen C Y, Baker S, Darton R. The application of a high throughput analysis method for the screening of potential biosurfactants from natural sources[J].Journal of Microbiological Methods,2007,70(3):503-511.
����[14]Altintas Z, Uludag Y, Gurbuz Y, et al. Development of surface chemistry for surface plasmon resonance based sensors for the detection of proteins and DNA molecules[J].Analytica Chimica Acta,2012,7(12):138-144.
����[15]Liu X. Performance Improvement for the Wavelength Modulation Surface Plasmon Resonance and Its Application[D].Changchun:Jilin University,2006.
����[16]����,������,������,��.��������ӹ������ﴫ������ʳƷ����е�Ӧ��[J].�������ѧ��,2012,22(4):73-76.
����[17]Hu J D, Chen R P, Wang S, et al. Detection of Clenbuterol Hydrochloride Residuals in Pork Liver Using a Customized Surface Plasmon Resonance Bioanalyzer[J/OL].PLOS ONE,2015,10(3):e0122005.
����[18]ʯ��,���,�����,��.����SPR���ﴫ�����Ŀ����ز�����⼰Ӱ�����ط���[J].����ѧѧ��,2010,43(3)255-261.
����[19]Edward L, Fafara A, Vandernoot V, et al. Surface plasmon resonance sensors using molecularly imprinted polymers for sorbent assay of theophylline, caffeine, and xanthine[J].Canadian Journal of Chemistry,1998,76(3):265-273.
����[20]Anand S, Usha S, Gupta B. Fiber optic profenofos sensor based on surface plasmon resonance technique and molecular imprinting[J].Biosensors and Bioelectronics,2016,5(79):150-157.
����[21]Zhang L L, Zhu C C, Chen C B, et al. Determination of kanamycin using a molecularly imprinted SPR sensor[J].Food Chemistry,2018,266(15):170-174.
����[22]LonL A, Musiek M. D, Natan M. J. Colloidal Au-Enhanced surface plasmon resonance immunosensing[J].Analytical Chemistry,1998,70(24):5177-5183.
����[23]Lee W, Son T, Lee C, et al. Ultra-Sensitive Surface Plasmon Resonance Detection by Colocalized 3D Plasmonic Nanogap Arrays[J].Biosensors and Biodetection,2017,3:15-29.
����[24]Lee S J, Youn B S, Park J W, et al. SSDNA aptamer-based surface plasmon resonance biosensor for the detection of retinol binding protein 4 for the early diagnosis of type 2 diabetes[J].Analytical Chemistry,2008,80(8):2867-2873.
����[25]Bianco M, Sonato A, De Girolamo A, et al. An aptamer-based SPRpolarization platform for high sensitive OTA detection[J].Sensors and Actuators B:Chemical,2017,3(241):314-320.
����[26]Wang S, Dong Y Y, Liang X G. Development of a SPR aptasensor containing oriented aptamer for direct capture and detection of tetracycline in multiple honey samples[J].Biosensors and Bioelectronics,2018,109:1-7.
����[27]�ۿ�,������,������.�����ش��Ĺ��ѧ���м����½�չ[J].������ѧѧ��,2017,33(5):729-735.
����[28]Hu J D, Li W, Wang T T, et al. Development of a label-free and innovative approach based on surface plasmon resonance biosensor for on-site detection of infectious bursal disease virus(IBDV)[J].Biosensors and Bioelectronics,2012,31(1):475-479.
����[29]Hu J D, Wang T T, Wang S, et al. Development of a surface plasmon resonance biosensing approach for the rapid detection of Porcine Circovirus Type2 in sample solutions[J/OL].PLOS ONE,2014,9(10):e111292.
����[30]Wang Y X, Ye Z Z, Si C Y, et al. Subtractive Inhibition Assay for the Detection of E.coli O157:H7 Using Surface Plasmon Resonance[J].Sensors,2013,11(3):2728-39.
����[31]Naboka A, Al-Rubaye A G, Al-Jawdah AM, et al. Novel optical biosensing technologies for detection of Mycotoxins[J].Optics and Laser Technology,2019,109:212-221.
����[32]�ܴ���,�³���,���,��.�յ����ӡ����������ӹ��������Ʊ������[J].Ӧ�û�ѧ,2014,31(19):1107-1114.
����[33]������,������,������,��.����������干�����ﴫ�����Ĺ����������ʻƵļ��[J].������ѧ�о�����,2014,42(1):53-58.
����[34]Pang K, Dong W, Zhang B, et al. A Performance-Enhanced Bimetallic Chip for the Detection of Cadmium Ions with Surface Plasmon Resonance[J].Plasmonics,2016,11(4):1119-1128.
����[35]Pelossof G, Telvered R, Willner I. Amplified surface plasmon resonance and electrochemical detection of Pb2+ions using the Pb2+-dependent DNAzyme and hemin/G-quadruplex as a label[J].Analytical Chemisry,2012,84(8):3703-3709.
����[36]Ф�ر�.���ñ�������ӹ���(SPR)���ﴫ�������ת���������о�[J].����ѧ,2009,17(2):38-43.
����[37]������,��ΰ,κ����,��.��ѧ��������ӹ������ﴫ�������С��ת������о�[J].����ũҵ��ѧѧ��, 2013,47(5):580-583.
����[38]Nasrin F, Chowdhury A D, Takemura K, et al. Single-step detection of norovirus tuning localized surface plasmon resonance-induced optical signal between gold nanoparticles and quantum dots[J].Biosens Bioelectron,2018,30(122):16-24.
����[39]Chiu N F, Yang C D, Chen C C, et al. Stepwise control of reduction of graphene oxide and quantitative real-time evaluation of residual oxygen content using EC-SPR for a label-free electrochemical immunosensor[J].Sensors and Actuators B,2018,258:981-990.
����[40]Otipka P, Vl?e J, Le��ák M, et al. Design of MO-SPR sensor element with photonic crystal[J].Photonics and NanostructuresFundamentals and Applications,2018,31:77-80.
����[41]Liu H, Wang M, Wang Q, et al. Simultaneous measurement of hydrogen and methane based on PCF-SPRstructure with compound?lm-coated side-holes[J].Optical Fiber Technology,2018,45:1-7.
����[42]Meyer Stefan A, AuguiéB, Le Ru Eric C, et al. Combined SPR and SERS microscopy in the Kretschmann configuration[J].Journal of Physics,2012,116(3):1000-1007.
ʳƷ���\�����ĵڶ�ƪ����ͬ�����ඹ��Ʒ�����ﰷ�ĺ�������
����ժҪ��Ŀ�� ���鸯�顢�����Ͷ���3�ඹ��Ʒ�����ﰷ����,�����˽ⷢ�Ͷ���Ʒ�����ﰷ������������� ����GB 5009.208-2016��ʳƷ��ȫ���ұ�ʳƷ�����ﰷ�IJⶨ��,���ø�ЧҺ��ɫ���ⶨ6�ָ��顢3�ֶ�����6�ֶ����е����ﰷ��������� �����е����ﰷ�������Գ���������,�������ﰷƽ��������472.35 mg/kg;�����Ը��ڶ���,�ֱ�Ϊ196.77 mg/kg��171.46 mg/kg�����顢�����Ͷ�����Ʒ�к�����ߵ����ﰷ�����Ұ�,������Ʒ�о���ε��Ǹ���,�����Ͷ�����Ʒ�������㰷,3��Ʒ����Ʒ�Ǿ����;������������١����� ���������, 3��Ͷ���Ʒ���ﰷ�����ڰ�ȫ��Χ�ڡ�
�����ؼ��ʣ����Ͷ���Ʒ; ����; ����; ����; ���ﰷ;
����Investigation and analysis of biogenic amines in different fermented bean products
����LI Xuan LIU Qi ZHU Wei-Shan CHEN Jing ZHANG Pei-Na JIANG Li-Wen
����Hunan Provincial Key Laboratory of Food Science and Biotechnology College of Food Science and Technology, Hunan Agricultural University
����Abstract��Objective To investigate the content of biogenic amines in 3 types of soybean products, such as sufu, soybean paste and fermented soybean paste, and to understand the existence of biogenic amines in fermented soybean products. Methods According to GB 5009.208-2016 National Food Safety Standard-Determination of Biogenic Amine in Food, the content of biogenic amines in 6 kinds of sufu, 3 kinds of soybean paste and 6 kinds of fermented soybean paste was determined by high performance liquid chromatography. Results The content of biogenic amines in sufu was obviously higher than that of the other two types, with the average content of total biogenic amines reaching 472.35 mg/kg. The biogenic amines in soybean paste with 196.77 mg/kg were slightly higher than those in fermented soybean paste with 171.46 mg/kg. The biogenic amines with the highest content in sufu, fermented soybean paste and soybean paste were tyramine, the second was putrescine in sufu, octopamine in fermented soybean paste and fermented soybean paste, and the spermidine and spermine contents in the samples of the three varieties were less. Conclusion On the whole, the biogenic amines in the three fermented bean products were within a safe range.
����1 ����
�������ﰷ��һ�����������Եġ��������ĵͷ��������л�����ܳ�,����֬���尷�������尷�Լ��ӻ���3��[1]���������ﰷ��������һ���ô�,����ǿ���������ٽ���������������,���������ﰷ��������������,����Ż�¡�ͷ�۵Ȳ���������Ӧ[2,3]�����ﰷ�Ĵ�����Ҫ�ǵ����ʷḻ��ԭ���綹�ࡢ������Ʒ��������ͺ�ˮ������������,�ڷ����������ת��ø��ǰ���»Ὣ������ת��Ϊ���ﰷ,��������Ʒ���ﰷ�����������о�ѧ�߹�ע��
��������ʳƷ�����ﰷ�ļ�ⷽ����������������ƴ�ʩ�ȷ�����о��϶ࡣ����ϵ�[4]�Ż����Ե���������Ϊ�����Լ������ʳƷ�����ﰷ�ķ���������־��[5]���ø�ЧҺ��ɫ���ⶨ�����ڲ�ͬ�¶��µ������ȥ��������г�����8�����ﰷ�Լ������ﰷ����,̽���¶Ⱥ�Ԥ���������������ﰷ�����仯��Ӱ�졣����ΰ��[6]���ַ��ն����ﰷ��������һ������������,�������ﰷ����ͷ���ǿ�ȵı仯���ó̶ȴ�С��һ�����������ﰷ����϶ࡢ��л;�����ӡ������ת����,���ﰷ������������ȷ����Ŀǰ,���ҽ��������ﰷ�ļ�ⷽ�����ұ�,����Ҫ�����ˮ��Ʒ���Ұ����鰷�ĺ���[7,8,9]��
�������ʹ���Ʒ�Ե����ʷḻ�Ĵ�����Ϊ��Ҫԭ�Ϸ��ͺ���,���ζ���ض��Ҿ��нϸߵ�Ӫ����ֵ,�������������ʳ�������벻�����Ͷ���Ʒ�����Ͷ���Ʒ��Ҫԭ�ϴ�,���ڼӹ����ղ��Ͳ�Ʒ��̬��ͬ,�ж��������顢������Ʒ��,�������������������������Ҫ�����ϳ��ķ���ʱ��(����һ��������),�������������и��ӵ�����������볤ʱ�䷢�͵�����ʹ���Ͷ���Ʒ�����ﰷ���ڿ���������,��˶��ڶ���Ʒ�����ﰷ�����ĵ������ʮ����Ҫ�����塣
�������о����г��ϳ����ĸ��顢�����Ͷ���3�ඹ��Ʒ�е����ﰷ�������з�������,��ⲻͬ��Ʒ�����ﰷ�������,�Ա��һ����߸��Ʒ��Ͷ���Ʒ����������ȫ��,Ϊ�����Ʒ�����ﰷ�Ĵ��ڼ����ܵİ�ȫ�������ƶ��ṩ�ο���
����2 �����뷽��
����2.1 ��Ʒ��Ϣ
�����ӳ��вɹ���6�ָ��顢6�ֶ�����3�ֶ���,���и����а���ͺ츯��,��1(S1)����5(S5)����6(S6)Ϊ����,��3(S3)Ϊ������,��4(S4)Ϊ������,��2(S2)Ϊ�ɸ���;��7(S7),��8(S8),��9(S9)Ϊ����,���̬��״;������Ϊ�ɶ�����ˮ�������Ͷ���,������10(S10)��11(S11)��12(S12)��13(S13)��Ϊ�ɶ���,��14(S14)Ϊˮ����,��15(S15)Ϊ�Ͷ���;��Ʒ������Ϣ����1��
����2.2 �������Լ�
����XW-80A���л����(�Ϻ����ֻ���������);Agilent1260��ЧҺ��ɫ���ǡ�ZORBAX SB-C18 Agilentɫ����(����Agilent��˾)��
��������(ɫ�״�)��������(������)����ˮ����(������)�����ȼ���(������)(��ҩ���Ż�ѧ�Լ�����˾);��ͪ(ɫ�״�,�人��ŵ��ʩ��˾);������(ɫ�״�,����л�ѧ�Լ��о�������˾)��
����2.3 �ⶨ����
��������GB 5009.208-2016��ʳƷ��ȫ���ұ�ʳƷ�����ﰷ�IJⶨ��[10]��һ��Һ��ɫ�����С�
����2.4 ���ݴ���
����ÿ�������ظ�3��,��EXCEL 2010�����ݽ���ͳ��ѧ����,�������X±R��ʾ��
����3 ��������
����3.1 Һ��ɫ����
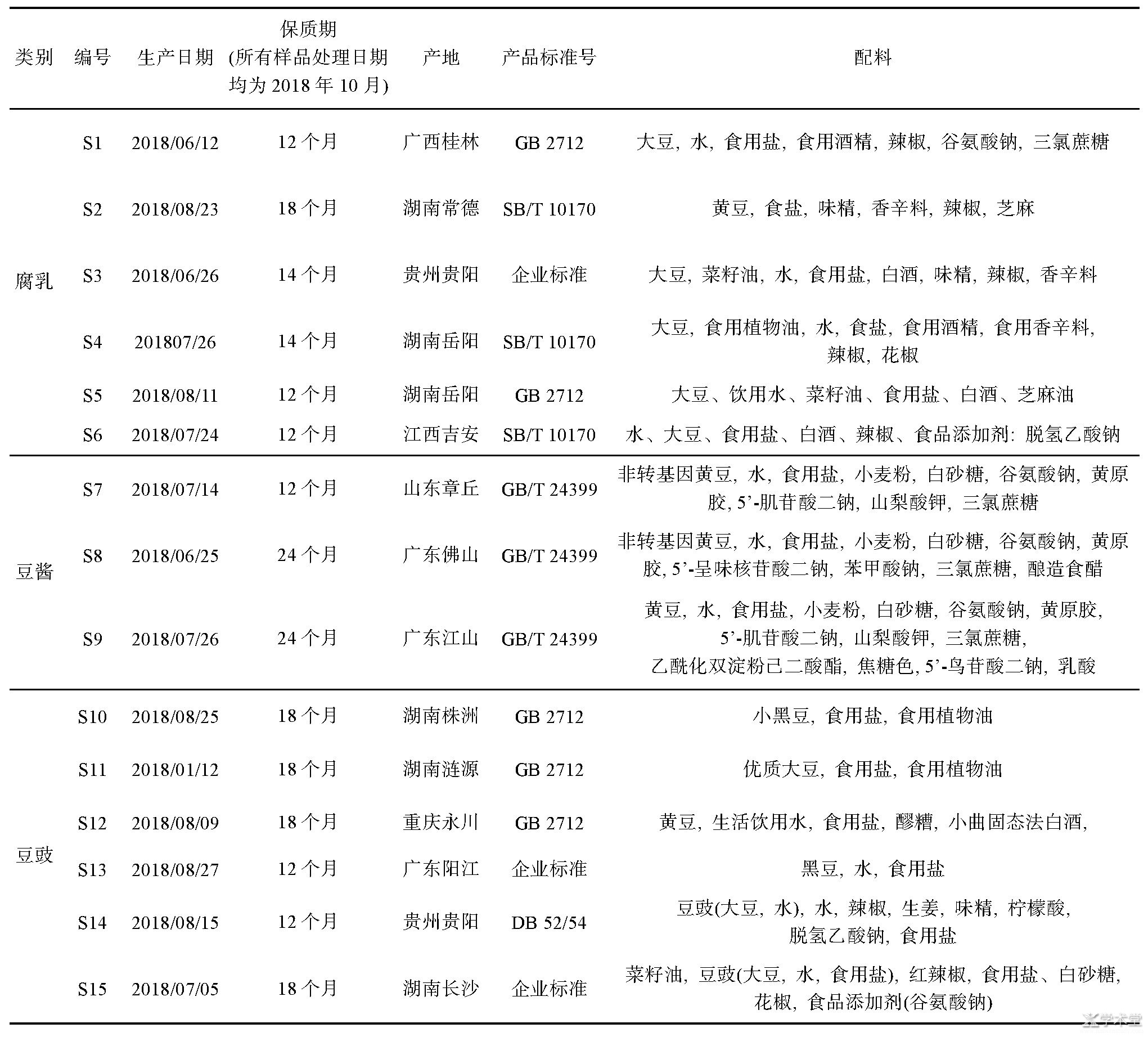
�������ȶԸ������ﰷ��Ʒ�ֱ����ɫ����,ȷ�������ʱ��,Ȼ��������ϱ�Ʒ���з���,���ɫ��ͼ��ͼ1��ʾ����ͼ1��֪,����Ʒ���ﰷ����ʱ����10��35 min֮��,���1��10�ֱ�Ϊɫ�������Ұ���������ʬ�����鰷�����㰷���ڱꡢ�Ұ����Ǿ����;�����3��ʵ����Ʒ��ɫ��ͼ��ͼ2��4��
����3.2 �����ﰷ�����Թ�ϵ
������2Ϊ����Ʒ���ﰷ���Թ�ϵ���ɱ�2��֪,�����㰷��,�����Ʒ���ϵ������0.9990����,˵���÷������ܶȽϺá����㰷�ǹ���İ��ż����,��ǰ�Ĺ��겢δ�������㰷�IJⶨ,��������ͬ����Ʒ���Ҳ�ͬ,���ݲⶨ�����ƫ��,������㰷���ϵ�����Ǻܺ�,ֻ����Ϊ�ο���
����3.3 3��Ͷ���Ʒ�����ﰷ�������
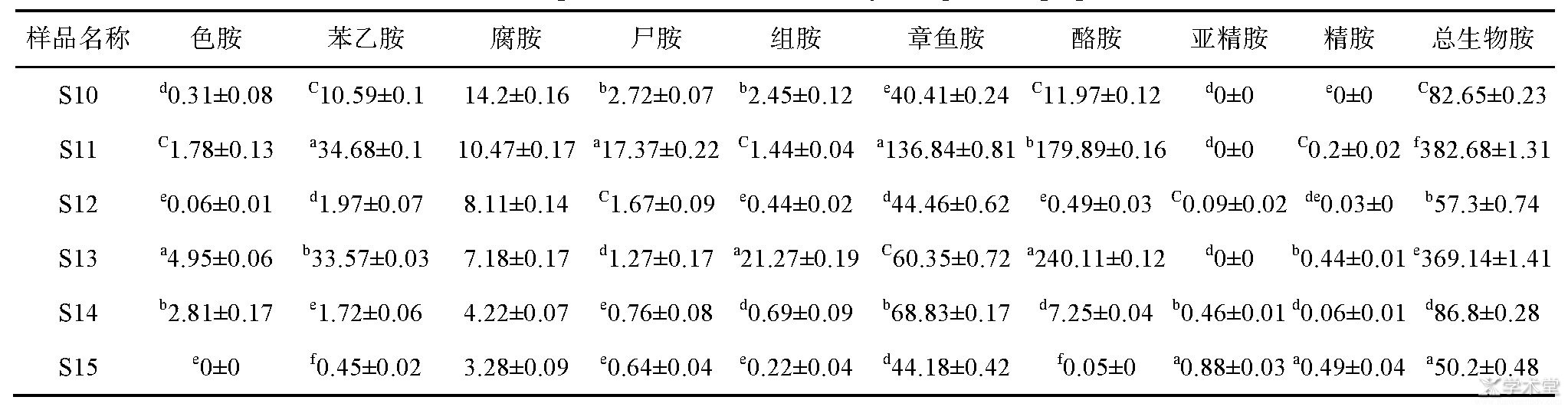
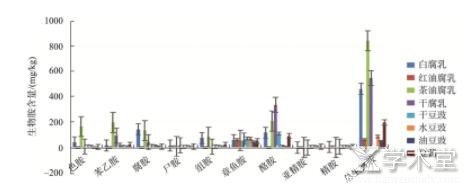
����������Ʒ��6�ָ��顢3�ֶ�����6�ֶ���,����10�����ﰷ����ͼ5,���и������ﰷ�������Գ�����2��,�������ﰷƽ��������472.35 mg/kg;�����Ը��ڶ���,�ֱ�Ϊ196.77 mg/kg��171.46 mg/kg���������в�����������ﰷ����Ϊ841.74 mg/kg,���ں�����(61.71 mg/kg)�Ͱ���(222.94 mg/kg)���������е�ɫ���ͱ��Ұ��ĺ���Ҳ�����������з��Ͷ���Ʒ������Ȼ��[11]���ָ�����ˮ����С�ĺ������ڶ���,�����Ϊ���������ﰷ���γ��ṩ�˸�����ͬʱ,���������ﰷ�����ߵ�ԭ��Ҳ��������ԭ���йء������ԭ���Ƕ���,�����Ͷ�����ԭ���Ǵ�,���֮��,����������(ëùΪ��)��øϵ�Դ�����ˮ��̶ȸ��ӳ���,��Ʒ������ӷḻ,���백���Ậ��Խ��,�γ����ﰷ�ļ���Ҳ��Խ��,���ϸ������û��ɱ������,����ϸ������Эͬ���ý�һ���ֽⰱ�����������ﰷ��
������1 ��Ʒ��Ϣ
��
��
��
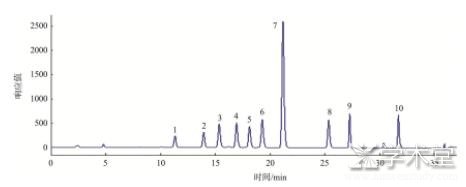
����ͼ1 ��ϱ�Ʒɫ��ͼ
��
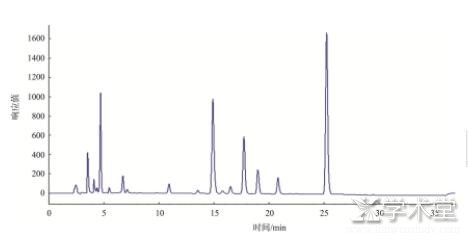
����ͼ2 ��1�����ɫ��ͼ
����
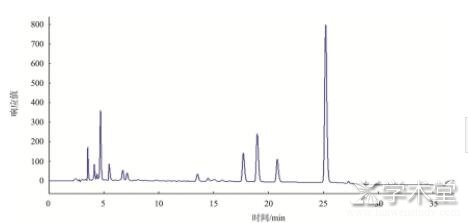
����ͼ3 ��8����ɫ��ͼ
��
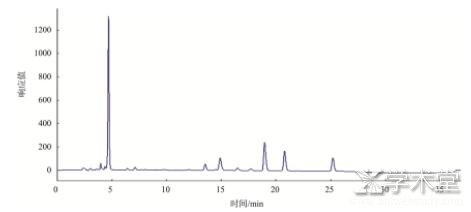
����ͼ4 ��10����ɫ��ͼ
����4�ฯ�顢3�ඹ���Ͷ����к�����ߵ����ﰷ�����Ұ�,���иɸ����е��Ұ����Ը����������з��Ͷ���Ʒ��8����Ʒ���Ǿ����;������������١����顢�����Ͷ����к�����ߵ����ﰷ�����Ұ�,�����о���ε��Ǹ���,�����Ͷ������������㰷,3��Ʒ����Ʒ�Ǿ����;�������������,�Ұ����Ƿ��Ͷ���Ʒ�д��ڽϸߵ�һ�ְ�����,�����������Ұ���ᾧ��(����),Ϊ�Ұ����γ��ṩ��Ҫǰ������,�������������γɡ����ﰷ���γ���������Ⱦ�̶���ѿ�߸˾����ٵ������ȴ����й�[12,13]�����о�����,�¶ȿ���Ӱ���鰷���γ�,��14����������ϸ�����Է����鰱������ø[14]�����3��Ͷ���Ʒ�����ﰷ����IJ���������������йء�
����3.4 ��ͬ���������ﰷ�����������
�����ӱ�3��֪,��ͬ������Ʒ���ﰷ���༰�������ڽϴ����,�������ԭ���������ԭ�ϡ��������ա����;��ּ�����ʱ���[15]�йء�S3Ϊ������,�ӱ���֪6�ָ����к��������ﰷ�������,��Ϊ61.74 mg/kg,����������10�����ﰷ��ֻ����ʬ�������㰷�;���,��ʬ���;���������,����������к����Ұ����鰷��δ���,�Ʋ�������п������������ﰷ�ϳɵ����ʴ��ڻ������ӹ���������Ч�������ﰷ�ϳɡ�����ɸ���(S2)�����ƴ�ͳ�մ�̳����,û�м���֭����,ˮ�ֺ�������������ָ����Ե�,���Ұ��������Խϸ�,ֵ�ý�һ��̽����
����3.5 ���������ﰷ�����������
�����ӱ�4��֪,3��������Ʒ�鰷���Ұ������㰷�϶�,����S9�ƶ������ﰷ��������,��Ҫ�����Ұ������������2����Ʒ���١���������һ����ûƶ������Ϊ��Ҫԭ��,����ùΪ��Ҫ���ͼ�,���Ҷ���һ����ñ��·��ͺ���Ȼɹ��,�������¶��ʺ��Ұ�������ø�����йء�������ԭ���䷽,���ƺ���Ʒ����һ����������,��˵���������ͳ�����Ʒ���ﰷ���ܻ���ߡ�����ŷ�˹涨,ʳƷ���Ұ��������ó���100��800 mg/kg,3�ֶ�����Ʒ����һ������100 mg/kg���ҹ����ڶ������Ұ�����������δ�����Ĺ涨,�䰲ȫ���д�̽����
������2 ��Ʒ���Թ�ϵ
����

����ͼ5 ����Ͷ���Ʒ���ﰷ����(n=3)
����3.6 ���������ﰷ�����������
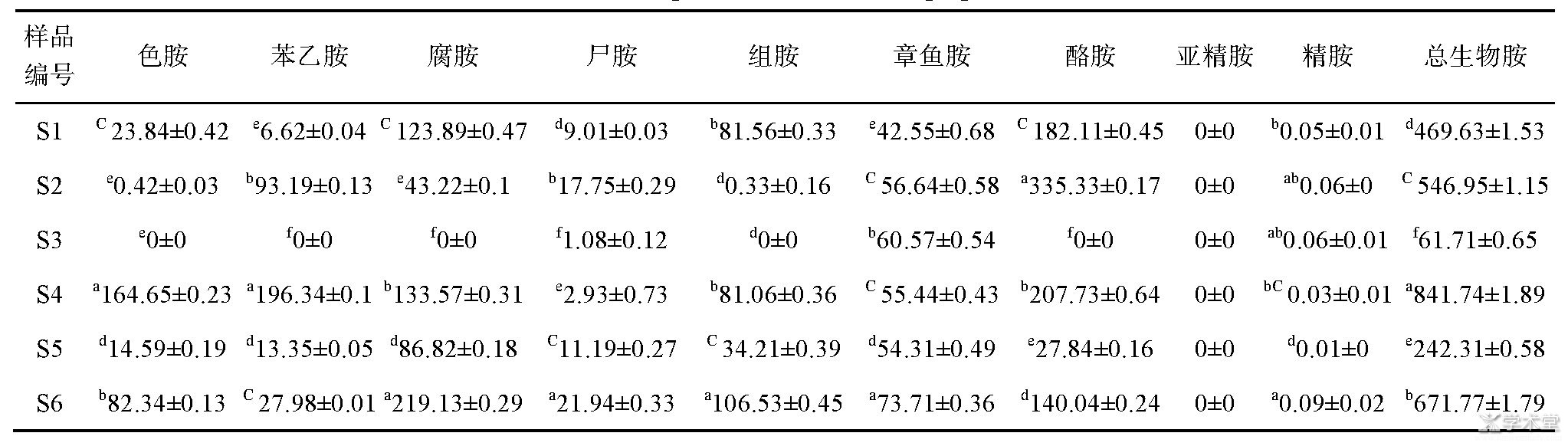
�������������ﰷ�����������5,6�ֶ�����S11��S13��2�ָɶ��������ﰷ�����ϸ�,��Ҫ��2�ֶ����Ұ������ϸ�,���S11�����㰷�����ϸߡ�S13���鰷�����ϸߡ����Ұ���[16]���ִ��ַ��������ﰷ����Ҫ������Ȼ����,���ʷ��[17]���ֲ�ͬëù������ù���������������ﰷ������ͬ,���ﰷ����ͺ�����������������й�,�Ʋ����������Ʒ�����ﰷ����������䷢�������������йء��������,ˮ�ֺ����ϸ��Ҿ���ζ�Ķ���(S14��S15)�ȸɶ���(S10��S11��S12��S13)���ﰷ����Ҫ��,���ܶ������ͳ�����ڼӹ���Ӱ�������ﰷ����,��������������,������������һ��̽����
������3 ������Ʒ�����ﰷ����(mg/kg,n=3)
����ע:��ͬ��ĸ�����������Բ���(P<0.05)��
������4 ������Ʒ�����ﰷ����(mg/kg,n=3)

��
����ע:��ͬ��ĸ�����������Բ���(P<0.05)��
������5 ������Ʒ�����ﰷ����(mg/kg,n=3)
����ע:��ͬ��ĸ�����������Բ���(P<0.05)��
����4 ����
�����������Ͽ�,����Ͷ���Ʒ�����ڰ�ȫ��Χ��,���Դ���ijЩƷ�Ʒ��Ͷ���Ʒ���ﰷ����ƫ��,�����dz���ŷ�����涨�����ﰷ�������ó���100��800 mg/kg���������ҹ���δ�ƶ���Ӧ��,������˵������Σ��,ֻ���Ʋ����һ�����ա����,���ε��鷢�ֺ��������ﰷ��������ƫ��,�������Ұ����鰷��δ���,��������ֵ�ԭ��ֵ��̽����
�������ܶ��������顢�������Ƿ��Ͷ���Ʒ,��ԭ����ȼ�����״̬(�����������)��������Ҫ�����Ʒ���������ﰷ�γ������й�ϵ�������е��������Ϊ��ù������ëù����,����ϸ��Ϊ���������[18,19],��ͬ���ͷ�ʽ�Ľ�������ϸ�����ڲ���,��ͬ�ַ��ͷ�ʽ�µĽ���������ϵ����[20];�����е���������ǽ�ĸ������ù����,����ϸ����ѿ�߸˾�Ϊ��[21];�����е�ϸ������������������ٵ�������������˾�����[22,23,24],�������Ҫ�������ֵ�ù�������Ͷ���Ʒ�����ﰷ��Ҫ�ɲ�����������ø���������ö�����[25]�����������о���֪,ʳƷ�������ﰷ������ص���Ҫ�����Ⱥ�мٵ�����������������ͳ������[26,27]���������Ϊ��,����������Խ�ǿ,����pH�ϵ�ʱ�ܲ�������İ���������ø��������绷���ı仯,���ص��뷢��ʳƷ������������һ�¡������ﰷ�Ŀ��Ƴ���,�Է��Ͷ���Ʒ��������о�ʮ�ֱ�Ҫ��
���������
����[1]����ǿ,�ὣ��,����,��.ʳƷ�����ﰷ���о���չ[J].ʳƷ��ѧ,2016, 37(1):269-278.Wang GQ, Yu JS, Hu J, et al. Progress in research on biogenic amines in foods[J]. Food Sci, 2016, 37(1):269-278.
����[2] Broadley KJ. The vascular effects of trace amines and amphetamines[J].Pharm Ther, 2010, 125(3):363-375.
����[3]����,���,��˽�.ʳƷ�����ﰷ�İ�ȫ���о���չ[J].ʳƷ��ѧ,2013, 34(5):322-326.Liu J, Ren J, Sun KJ. Research progress on safety of biogenic amines in food[J]. Food Sci, 2013, 34(5):322-326.
����[4]���,�ƺ���,�̳ɸ�,��.���ﰷ�����������������Ż��о�[J].ʳƷ�뷢�ͿƼ�, 2018, 54(1):45-49.Wu D, Huang HJ, Cai CG, et al. Study on optimization of conditions for derivatization of biogenic amine with dansulfonyl chloride[J]. Food Ferment Technol, 2018, 54(1):45-49.
����[5]����־,�˽���,������,��.��ͬ�����¶����������ﰷ�仯���о�[J].ʳƷ��ҵ�Ƽ�, 2018, 39(4):260-267, 279.Zhao QZ, Deng JC, Yang XQ, et al. Changes of biogenic amines in mackerel under different storage temperatures[J]. Sci Technol Food Ind,2018, 39(4):260-267, 279.
����[6]����ΰ,�ۺ��,���Ʊ�,��.���ն����ع����д�ܱ�Ϻ���ﰷ�γɵ�Ӱ��[J].�й�ʳƷѧ��, 2018, 18(1):176-183.Xiang XW, Shao HH, Hao YB, et al. Effect of irradiation on biogenic amine formation in solenocera melantho during storage[J]. J Chin Inst Food Sci Technol, 2018, 18(1):176-183.
����[7] GB 2733-2005�ʡ���������ˮ��Ʒ������[S].GB 2733-2005 Hygienic standard for fresh and frozen animal aquatic products[S].
����[8] US Food and Drug Administration. CPG Sec. 540. 525 Decomposition and histamine raw, frozen tuna and mahi-mahi, canned tuna; and related species, revised compliance policy guide, availability[Z].
����[9] European Commission(EC). Commision recommendation of 10 January2003 concerning a coordinated programme for the official control of foodstuffs for 2003(2003/10/EC)[Z].
����[10] GB 5009.208-2016ʳƷ��ȫ���ұ�ʳƷ�����ﰷ�IJⶨ[S].GB 5009.208-2016 National food safety standard-Determination of biogenic amines in food[S].
����[11]����Ȼ,������,�O����,��.��������Ʒ��ˮ��������������ʵķ���[J].�й�ʳƷѧ��, 2016, 16(2):258-265.Li YR, Zhao LQ, Yun TT, et al. Analysis of water-soluble bioactive substances in common soybean products[J]. J Chin Inst Food Sci Technol,2016, 16(2):258-265.
����[12] Jin SM, Seung KC, Hwa YC, et al. Isolation and characterization of Biogenic Amine-producing Bacterium in fermentated soybean-paste[J]. J Microbiol, 2010, 48(2):257-261.
����[13] Tsai YH, Kung HF, Lee YH, et al. Histamine contents and histamine-forming bacteria in sufu products in Taiwan[J]. Food Control,2007, 18(5):381-387.
����[14]����,������,�۽�ȫ,��.�й���ͳ���Ͷ��������ﰷ����[J].ʳƷ��ѧ, 2013, 34(20):108-112.Hu P, Suo HY, Kan JQ, et al. Biogenic amine content of traditionally fermented Douchi[J]. Food Sci, 2013, 34(20):108-112.
����[15]�����,κ����,�Ž���,��.��ЧҺ��ɫ������й���ͳ���Ͷ�����Ʒ�е����ﰷ[J].�й�ʳƷѧ��, 2010, 10(4):253-259.Liu ZF, Wei YX, Zhang JJ, et al. Determination of biogenic amines in Chinese traditional fermented tofu products by high performance liquid chromatography[J]. J Chin Inst Food Sci Technol, 2010, 10(4):253-259.
����[16]���Ұ�,������,���,��.���������ﰷ�����Ķ�̬�仯�о�[J].�й�����, 2016, 35(5):60-64.Han ZA, Luo XX, Yang CY, et al. Dynamic changes of biogenic amines content in Douchi[J]. Chin Brew, 2016, 35(5):60-64.
����[17]���ʷ�,�¹⾲,������,��.�������ͳ���ëù������ù��������ﰷ����������[J].ʳƷ�뷢��ҵ, 2017, 43(9):15-21.Zhang RF, Cheng GJ, Yang WM, et al. Evaluation of biogenic amines produced by Mucor and Aspergillus oryzae in Douchi fermentation process[J]. Food Ferment Ind, 2017, 43(9):15-21.
����[18]����.��Ȼ���Ͷ�����������Լ�Ʒ�ʷ���[D].����:����ũҵ��ѧ, 2018.Jiang J. Analysis on microbial diversity and quality of naturally fermented soybean paste[D]. Shenyang:Shenyang Agricultural University, 2018.
����[19]������,������,��ƽ,��.�����붹�������ϵ�о�[J].ʳƷ��ҵ�Ƽ�, 2019, 40(7):101-106, 113.Zhang PF, Wu RN, Zhang P, et al. Study on the microbial relationship between fermented grains and soy sauce[J]. Sci Technol Food Ind, 2019,40(7):101-106, 113.
����[20]����,����ϫ,������,��.Ӧ��MiSeq���������Ȼ���Ͷ�������������Ķ�����[J].ʳƷ��ҵ�Ƽ�, 2018, 39(16):92-97.Jiang J, Xie MX, An FY, et al. Analysis of microbial diversity in naturally fermented soybean paste by MiSeq[J]. Sci Technol Food Ind, 2018,39(16):92-97.
����[21]����,��Ƽ,��Ƽ,��.���ݶ�����������������о�[J].�й�����,2019, 38(3):81-88.Fan M, Yang P, Hu P, et al. Microbial diversity in Douchiba from Guizhou[J]. Chin Brew, 2019, 38(3):81-88.
����[22]��ӱ��. PCR-DGGE������ͬƷ�Ƹ�����ϸ���Ķ�����[J].�й���ζƷ, 2017, 42(7):29-32.Chen YH. Analysis of bacterial diversity in sufu from different brands by PCR-DGGE[J]. Chin Cond, 2017, 42(7):29-32.
����[23]���Ƕ�.����16S r DNA����ķ���������������������������[D].����:ɽ��ʦ����ѧ, 2017.Liu YD. Identification of microbial species diversity in sufu b 16S rDNA[D]. Jinan:Shandong Normal University, 2017.
����[24]��־��,����,�����.��ҵ��������������ķ��������[J].ʳƷ��ȫ����, 2018,(18):154-156.Zhang ZC, Luo JM, Yin GL. Isolation and identification of lactic acid bacteria from commercial sufu[J]. China Food Saf Magaz, 2018,(18):154-156.
����[25]���Dz�,�ィ��,������,��.ʳƷ�������ﰷ�γ���ص������Ⱥ������Ƽ����о���չ[J].ʳƷ��ѧ, 2018, 39(15):262-268.Jing ZB, Tian JJ, Yang MY, et al. Research progress on microbial flora related to biogenic amine formation in food and its control technology[J].Food Sci, 2018, 39(15):262-268.
����[26]������,���,��Ф,��.��ͳ��������Ʒ�����ﰷ�γɻ����������Ƽ���[J].�����о�, 2013, 27(6):39-43.Wang YL, Li F, Chen X, et al. Formation mechanism and detection and control technology of biogenic amines in traditional fermented meat products[J]. Meat Res, 2013, 27(6):39-43.
����[27]�ż���,����÷,���췽.�����ﰷ������о�����[J].ɽ��ũҵ��ѧ, 2014, 42(5):521-525.Zhang JM, Zhao YM, Xu QF. Review on the induction of producing amines of Lactic acid bacteria[J]. J Shanxi Agric Sci, 2014, 42(5):521-525.










 ��
��