
杏仁核又称杏仁复合体,是边缘系统的一个重要核团,包含十多个大小不同的核群,并可能作为重要的痛觉信息编码和调制的大脑中枢,不但在情绪认知记忆方面而且在情感障碍例如焦虑和忧虑方面都起着重要的作用.然而,最近的研究表明,在杏仁核的众多亚核群中,中央杏仁核(central amygdala, CeA)被认为是与痛觉活动相关的重要核团,它接受伤害性感受信息的传入,因而被认为是一个伤害性感受核团。CeA 中的大量神经元对伤害性刺激的反应具有“优先和独立”的特性.CeA 能够通过脊髓-臂旁核-CeA 痛觉通路接受单纯的伤害性信息,并通过这条通路与脊髓和脑干的伤害性感受中枢发生联系,从而参与内脏痛觉信息的传递。但 CeA 是否参与心脏痛觉信息的传递并是否对其具有调控作用,尚未见报道。本研究以心包内注射致痛物质诱发大鼠 SPT 放电为指标,通过观测 CeA 内 c-Fos 表达的变化及不同强度电刺激 CeA 后大鼠背斜方肌肌电反应(EMG)的变化,从而探讨 CeA 对大鼠心脏伤害性感受信息的传递及调节作用。
1 材料与方法
1.1 试剂与仪器 兔抗大鼠 c-Fos 多克隆抗体(美国 abcom 公司);ABC Kit免疫组化试剂盒(rabbit IgG,美国 Vector 公司);CAP(美国 Sigma 公司);常用试剂(本室配制);冰冻切片机(CM1900,德国 Leica 公司);Olympus 生物显微镜(BX51,日本 Olympus 公司);刺激器(SEN-3301,日本 Nihon Kohden公司);隔离器(SS-202J,日本 Nihon Kohden 公司);大鼠脑立体定位仪(SN-2N,日本 Narishige 公司);生物信号采集与分析系统(BL-420,成都泰盟生物科技有限公司)。
1.2 实验动物与分组 实验选用健康雄性、标准清洁级成年 SD 大鼠,体重 250~300g.随即分为正常对照组(n=6)、心包内注射生理盐水组(n=6)、心包内注射 CAP 组(n=6),电刺激 CeA 的强度分别为 30?A 和 70?A(n=6)(心包内注射 CAP 15s 后行 CeA 电刺激)。
1.3 方法
1.3.1 手术 实验动物称重后用 20mg/mL 戊巴比妥钠腹腔注射麻醉,行常规气管插管和颈静脉插管,于左侧上胸部第 1~3 肋软骨处行开胸术,暴露胸腺和心脏。将一远端有数个小洞的硅胶管(长 14~16cm、内径 0.020cm、外径 0.037cm)从此孔顺胸腺间隙插入心包腔内约 3~4cm,并逐层缝合胸腺和各层胸壁组织。心包内每次可注入的液体量约为 0.2mL 并能完全回吸。实验动物取俯卧位,暴露左侧 SPT,水平插入同芯电极,深度 1.5~1.7mm,用 BL-420 生物机能实验系统记录肌电活动。
1.3.2 免疫组织化学方法测定中央杏仁核 c-Fos 的表达 实验动物用 20mg/mL戊巴比妥钠深麻后打开胸廓,经主动脉灌流后取出大脑并固定,沉糖后进行脑部冰冻切片,切片厚 40?m.按以下流程依次进行操作:用 3mL/L 的过氧化氢溶液灭活内源性的过氧化物酶,用 0.3%的 PBS-T 通透,用 100mL/L 血清封闭液封闭,加一抗(1∶500,阴性对照实验中,用 PBS 代替一抗,)、二抗(1∶200)及A/B 液(0.3%的 PBS-T 1∶100,室温孵育 2h)。DAB 显色,裱片,脱水,透明,封片,用 Olympus 光学显微镜(BX51)及照相软件 SPOT 对脑部切片进行图像采集分析。用 Imag-Pro-Plus 软件计数 CeA 内的 c-Fos 阳性细胞数。每只大鼠 CeA位置取 5 张切片进行 c-Fos 阳性细胞计数并计算均数。
1.3.3 电生理学方法记录肌电反应 心包内重复注射 CAP 后大鼠背斜方肌 EMG的记录:记录正常对照组(即未给予任何处理)的 EMG 1min 作为基线活动,然后心包内注射 CAP(0.01g/L,0.2mL),记录肌电活动,1min 后回抽,用生理盐水冲洗心包腔 5~6 次(0.2mL/次),间隔 50min.如此反复 4 次心包内注射CAP.
不同强度电刺激 CeA 后大鼠背斜方肌 EMG 的记录:CeA 刺激电极置于前囟向尾 2.0~2.2 mm,右旁开 4.0~4.2mm,深度 7~9mm.刺激参数:频率为 50Hz,波宽为 0.2ms,刺激强度分别为 30?A 和 70?A;刺激时间均为 1min.记录 EMG基线活动 1min 后,再以心包内注射 CAP(0.01g/L,0.2mL)后记录的 EMG 活动作为基础对照,1min 后回抽并用温生理盐水冲洗心包腔;间隔 50min 行 CeA电刺激(30?A,15s),15s 后继续维持电刺激并且心包内注射 CAP(0.01g/L,0.2mL)记录 EMG,1min 后回抽并冲洗心包腔;间隔 50min 行 CeA 电刺激(70?A,15s),15s 后继续维持电刺激并给予心包内注射 CAP(0.01g/L,0.2mL),记录EMG,1min 后回抽并冲洗心包腔。
1.4 统计学处理 计量资料以 x ±s 表示,采用 SPSS 16.0 统计软件进行分析。
免疫组化采用 one-way ANOVA 并 SNK-q 检验进行分析;肌电反应采用重复测量的方差分析。P<0.05 为差异有统计学意义。应用图形可视化和数据分析软件SigmaPlot10.0 作图。
2 结 果
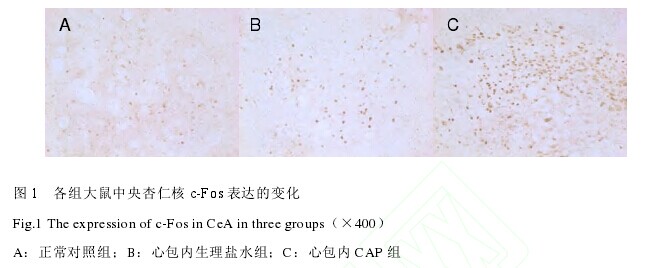
2.1 心包内 CAP 注射对中央杏仁核 c-Fos 表达的影响 统计结果表明,3 组之间有差别,c-Fos 阳性表达量在正常对照组(n=6)为 7.57±1.32,心包内生理盐水组(n=6)为 12.67±3.21,心包内 CAP 组(n=6)为:90.82±3.24.其中心包内生理盐水组与正常对照组相比,无统计学差异(P>0.05)。相反,心包内注射CAP 组诱发了 CeA 中大量 c-Fos 表达,其阳性细胞数明显高于心包内生理盐水组(P<0.05,图 1)。【图1】
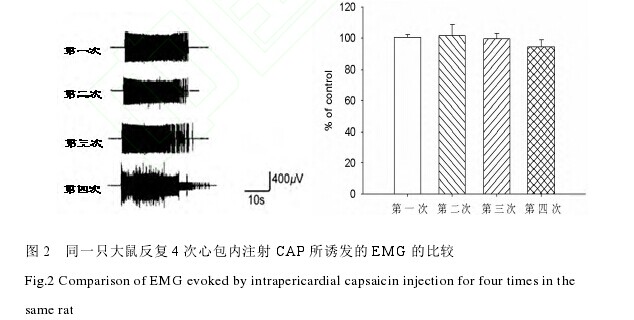
2.2 心包内注射 CAP 诱发的 EMG 具有可重复性 6 只大鼠心包内反复 4 次注射 CAP,每次间隔 50min.统计结果表明,第 2 次到第 4 次心包内注射 CAP 所诱发的 EMG 反应与第 1 次 CAP 刺激所诱发的 EMG(基础对照,100%)无明显差别。其标化率分别为(101.67±1.87)%、(99.47±2.37)%、(94.59±1.87)%,差异无统计学意义(P<0.05,图 2)。【图2】
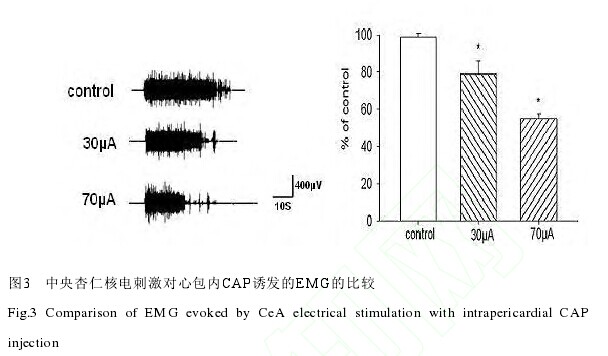
2.3 中央杏仁核电刺激对心包内 CAP 诱发的 EMG 的调节效应 电刺激 CeA的结果显示,30?A(n=6)电刺激 CeA 后心包内注射 CAP 诱发的 EMG 反应下降至基础对照值的(78.58±4.62)%(P<0.05);70?A(n=6)电刺激 CeA 后心包内注射 CAP 诱发的 EMG 反应下降至基础对照值的(54.89±3.98)%(P<0.05,图 3)。【图3】
3 讨 论
内脏中的感受器主要是痛觉感受器,因此内脏感觉主要是痛觉。内脏痛常由挤压、牵张等机械刺激、炎症和代谢产物等化学性刺激引起,其特点是疼痛缓慢而持久,定位不准确,以及情绪和自主神经反应等。当冠状动脉的供血量与心肌的需血量之间发生矛盾,即冠状动脉血流量不能满足心肌代谢的需要时,会引起心肌急剧的、暂时的缺血缺氧,即可发生心绞痛。心绞痛的典型表现为阵发性的前胸部压榨性疼痛感觉,主要位于胸骨后部,同时可以放射到颈部、臂部、颚或牙齿.关于心绞痛发生的信息传入途径,一般认为伴随心脏交感神经的感觉传入纤维,其末梢广泛分布于心室肌浅表层、心包膜脏层和部分壁层;传入纤维组成部分心下神经,经星状神经节投射至上胸段(T1~T5)脊髓背角,并与体表神经在脊髓内发生会聚联系,再通过丘脑传入到大脑皮质而产生痛觉.
已知大脑边缘皮质的中央杏仁核接受伤害性感受信息的传入,但迄今为止,有关 CeA 在心脏伤害性感受信息的传入及调节方面的研究鲜有报道。JOU 等人的研究发现,给大鼠心包内注射致痛物质可诱发 SPT 放电,这可以作为心脏-躯体运动反射(CMR)的指标,即心脏伤害性感受的反应指标,也是作为研究心脏伤害性感受传入和调控作用的简单有效的动物模型,藉此探索 CeA 与心脏伤害性感受传入之间的关系以及电刺激 CeA 对 CMR 的影响。
本研究通过心包内注射 CAP,制备大鼠 CMR 痛觉模型;采用免疫组织化学方法观察到心包内注射 CAP 可引起 CeA 中 c-Fos(即伤害感受神经元活动的标志物)阳性细胞数量明显增加,已知观察 c-Fos 在中枢神经系统的空间表达状况是探索伤害性感受信息传入及其神经通路最常用的方法之一,有研究表明,腹腔注射乙酸所致的内脏痛可使 CeA 的 c-fos mRNA 表达显着增加.在结肠炎痛觉的动物模型中,CeA 的 c-Fos 蛋白表达也均有所增加,说明 CeA 与内脏痛觉之间的确存在密切关系。近来,有研究发现通过对麻醉的老鼠行细胞外单个电位放电记录,从电生理活动分析了心脏伤害性信息的传递,结论显示 CeA神经元聚集有大量躯体感觉和内脏伤害性信息的传入信号.刺激猫的牙髓可以在 CeA 的内侧部和外侧部记录到对伤害性刺激发生反应的神经元,其反应可以被吗啡抑制,纳洛酮可以逆转这种抑制作用.从本研究的图 3 中可知,使用电生理方法研究发现电刺激CeA明显地抑制了由心包内注射辣椒素诱发的EMG反应,反映 CeA 可能参与了大鼠心脏伤害性感受信息的下行抑制性调控。但关于中央杏仁核参与心脏伤害性感受信息传递与调控的神经递质、受体及其信号转导机制如何,则有待进一步研究证实。





