题目:ELISA法检测乙肝表面抗原的方法学评价
目 录
摘要(详见正文)
关键词
前言
1 材料与方法
1.1 仪器和试剂
1.2 方法
1.2.1溶液的配制
1.2.2加样方法
1.2.3测定方法
1.2.4标准曲线制作及结果计算方法
2 结果
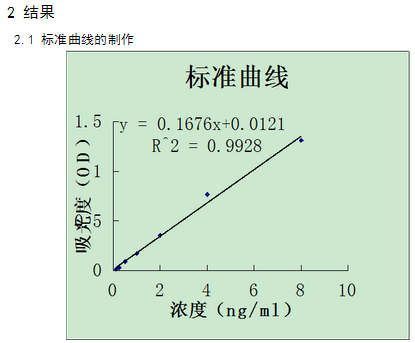
2.1 标准曲线的制作
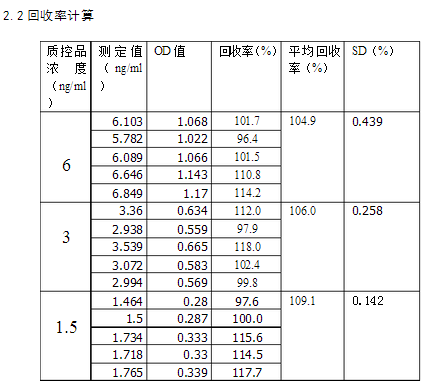
2.2 回收率结果
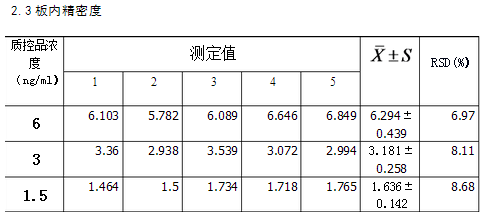
2.3 批内重复试验
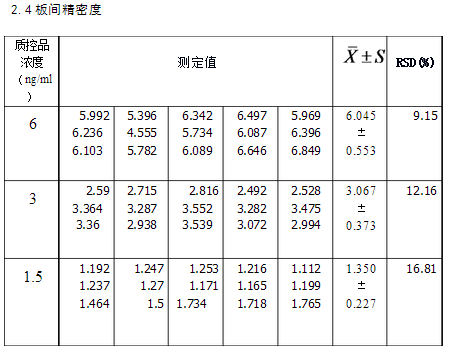
2.4 批间重复试验
2.5 检测限(LOD)计算
3 讨论
3.1 背景知识介绍
3.2实验结果分析
3.3实验中遇到的具体问题分析
3.4 ELISA中可能存在的假阳性结果
结论
参考文献
以下是正文
摘要:目的:对ELISA法定量检测乙肝表面抗原(HBsAg)进行方法学评价。方法:首先制定标准曲线,配制中,高,低,三种浓度的质控品,用ELISA法进行5次批内重复试验,与另外两组测定结果进行批间重复性测定,从而进行准确度和精密度的评估。结果:标准曲线回归方程为:y = 0.1676x+0.0121,相关系数 r = 0.9928.HBsAg检测的回收率(高值、中值、低值)分别为104.9%、106.0% 、109.1%;HBsAg批内重复性(高值、中值、低值)RSD分别为6.97% 、8.11%、8.68% ,批间重复性(水平1、水平2,水平3)CV分别为9.15%、12.16% 、16.81% ,均满足要求;结论:用ELISA法定量检测HBsAg,其准确度和精密度能够满足临床定量分析的要求。
关键词:乙肝表面抗原(HBsAg);方法学评价;ELISA法;定量检测
前 言
我国为乙型肝炎病毒感染的高流行区,正常人群的乙肝表面抗原(HBsAg)携带率一般为10%-15%。乙肝表面抗原(HBsAg)是乙肝病毒的外壳蛋白,本身不具有传染性,但它的出现常伴随乙肝病毒的存在,所以它是已感染乙肝病毒的标志。它可存在于患者的血液、唾液、乳汁、汗液、泪水、鼻咽分泌物、精液及阴道分泌物中。在感染乙肝病毒后2~6个月,当丙氨酸氨基转移酶升高前2~8周时,可在血清中测到阳性结果。急性乙型肝炎患者大部分可在病程早期转阴,慢性乙型肝炎患者该指标可持续阳性。乙肝表面抗原在乙肝诊断中具有重大意义,是临床上的一项常规检测。目前,检测乙肝表面抗原的方法有琼脂免疫扩散法、对流电泳法、反向被动血凝法(RPHA)、酶联免疫法、固相放射免疫法,国内检测HBsAg用得最为普遍的方法是酶联免疫吸附法(ELISA),本文用ELISA方法检测了质控品中HBsAg进行定量分析测定,井对其准确性、精密度进行了评价。
1 材料与方法
1.1 仪器和试剂
试剂盒:乙肝表面抗原ELISA法定量分析试剂盒,福州蓝图生物工程有限公司出品。 酶标仪:Bio-Rad 680 ; 洗板机:Bio-Rad 1575; 超纯水系统:Millipore Elix ; 电热恒温培养箱(DNP-9052):上海精宏实验设备有限公司;档位加样枪(10-50ul,100-500ul)各一支,1.5mlEP管 数个 试剂: 0.01M pH7.4的PBS缓冲液:称取8g NaCl、0.2g KCl、1.44g Na2HPO4和0.24g KH2PO4,溶于800ml蒸馏水中,用HCL溶液的pH值至7.4,最后加蒸馏水定容至1L即可。 8ng/ml的乙肝表面抗原标准品,质控品:用PBS缓冲液将标准品配制成6、3、1.5ng/ml三个 质控品。
1.2 方法
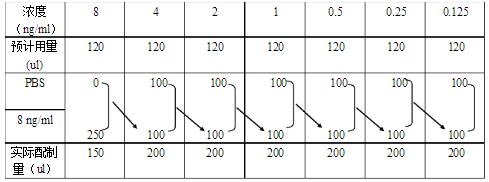
1.2.1 各浓度溶液的配制
用PBS缓冲液将8ng/ml的标准品配制成8、4、2、1、0.5、0.25、0.125ng/ml。
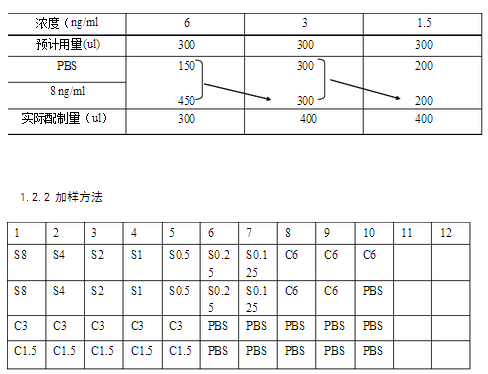
1.2.3测定方法
(1)设计标准品、质控品及空白分配方案;(质控品稀释方法:3份8ng/ml的标准平加入一 份PBS缓冲液,混匀所得6ng/ml.依次倍比稀释可得3,1.5ng/ml)
(2)取出试剂盒中已包被酶标板,取出板条,按需要重新配制;
(3)在相应孔中加入系列标准品、质控品及空白对照,每孔50ul;
(4)37℃温育30min,洗板4次;
(5)加入酶标抗体,生物素二抗,50 ul/孔;
(6)37℃温育30min,洗板4次;
(7)加入A、B液,50 ul/孔,37℃温育15分钟。
(8)加入终止液,50 ul/孔。
1.2.4 标准曲线制作及结果计算方法
酶标板放入酶标仪,盖上盖子;在电脑上打开Microplate Manager 5.2软件;选择450nm波 长(参照波长630nm),设置LAYOUT和报告模式,测定各孔吸收值;输入标准品各浓度值,以双对数法制备标准曲线,获取各孔的浓度值,打印标准曲线图和计算结果。
2.5检测限(LOD)计算:
取空白孔的OD值的均数加2倍标准差:OD值 0.0720 + 2 ×0.006=0.084
3.讨 论
3.1 背景知识介绍
HBsAg是乙肝病毒感染后最早出现的血清标志物之一,因此HBsAg的检测是诊断肝炎病毒感染的重要依据。乙肝病毒标志物中同时出现HBsAg、HBeAg和抗一HBc呈阳性反应,说明病人体内HBV复制活跃,传染性强,是临床最重要的乙肝传播者,在传染病学中有重要意义。特别是对献血员、孕妇、外科手术患者,更应引起足够重视。HBV病毒自身存在变异,急、慢性肝炎及重型肝炎出现前C区变异;HBV的S区变异常出现HBsAg阴性的HBV感染者 ,所以不能单纯以HBsAg结果而判定乙肝病毒的存在。在实际工作中检测HBV—M时我们应注意以下几点:特别是对HBeAg和抗一HBc呈阳性的血清标本应引起足够重视; 以检测五项为佳,尽可能地不单独检测HBsAg而据此判断病情;有条件时应同时检测HBV—DNA,以有效防止乙肝病毒血清的错检或漏检。现在乙肝表面抗原的检测,定性检测已经不能满足临床的需求了, 而定量检测HBsAg已经成为时代发展的必然趋势了,一般的乙肝表面抗原定量检测值大于0.18ng/ml时,就说明该患者体内的乙肝表面抗原为阳性结果,反之被以为是乙肝表面抗原阴性。 ELISA方法是目前临床上应用最广泛的方法,其方法的特异性和灵敏度已经得到早以得到证实两了,而要用于定量分析中最最要的指标有两个,精密度和准确度,故本实验设计的主要目的是对ELISA法定量检测HBsAg的精密度和准确度做方法学评价,检测系统的性能指标能否满足临床检测的要求会影响临床诊疗的效果。
3.2 实验结果的分析
本实验利用的是ELISA的方法来检测乙肝表面抗原,利用的是双抗夹心法,操作步骤上采用的是两步法,其目的是利用试剂盒来检测高,中,低三种不同浓度模拟的生物样品,每种样品进行了五次重复试验,通过七个标准品制定标准曲线,通过标准曲线,可以得到相同浓度的五个质控品的检测浓度,与实际加入浓度做比较计算回收率来评价准确度,利用五个值之间的差异求RSD从而来评价批内精密度,本组结果去其他组的进行必要来衡量批间精密度的大小。从实验的数据结果来看,标准曲线的浓度选择范围为8-0.125ng/ml的浓度范围,包括了临床大多数阳性病人的范围,从标准曲线的结果,看其相关性r>0.99,相关性较好符合实验要求,从其检测限度取空白孔的OD值的均数加2倍标准差:OD值 0.0720 + 2 ×0.006=0.084,低浓度的各质控品的OD值都大于了0.084故本实验的检测结果可靠,可以用于方法学分析。在进行准确度的评价过程中我们选取了三个浓度的模拟生物样品,分别是6,3,1.5 ng/ml。在标准曲线的线性范围内符合要求,从结果来看,中,高浓度的,各测定值的相对回收率都在85%-115%,回收率的平均均值也在85%-115%之内,低浓度样本的回收率为109.1%也在范围80%-120%之内,故从上述结果可知该方法的准确度较好能满足临床的需求,即是说用该方法检测所得的生物样品中的HBsAg浓度与其实际的浓度相接近。关于精密度,的评价指标为RSD,板内RSD高,中,低 三个浓度分别为6.79%,8.11%,8.68%均小于限度15%,板间RSD高,中,低 三个浓度分别为9.15%,12.16%,16.81%,由于第三个值应小于<20%满足要求,故该方法可重复性较好,其精密度符合临床要求。
3.3 实验中具体问题的分析
在具体实验操作过程中,有些问题值得注意,就是在操作加样过程做,无论是标准品还是质控品的用量一定要配制足够量的,因为,据我了解实验中,有些组就是在加样过程中只有发现了配制的质控品不够用,结果又进行了第二次配制,从比色结果来看其OD值相差两倍,特别是在低浓度的质控品时,还有就是实验室所用的档位加样枪比较粗犷,而且并没有定期的校准,所以使用时,我们尽量必要交叉使用加样枪,整个过程每种规格的就用一把枪,便于减少误差,也可以两个组在一起做,用相同的枪,相同的试剂,最后相同的步骤由专人操作,尽量减少人为操作因素的形象。虽然从实验结果来看准确度和精密度,都达到了质控的要去的范围内,但是明显的可以看到组内的数据,同浓度有个别值偏差较大,不同组间,精密度较好,但是组间同一浓度的质控品所得检测值存在差异,其中有很大原因还是操作引起的。同时在用ELISA法的时候一定要注意,到底是用一步法,还是两法,本实验之前一天的实验结果都并不是太理想,原因除了操作上引起的差距在外就是因为他们直接采用的一步法,加入标准品和质控品后,直接加进去了酶标二抗使标准品进一步稀释了,结果只有很少的部分与孔内固定的一抗反应,所以颜色偏低,导致OD值太小,浓度较低的孔如(0.5,1.5,0.125ng/ml)几乎没有什么颜色,接近于空白对照无法进行计算,实验失败,这提示我们,临床上很有可能有低水平HbsAg阳性携带者,无法检测出,还有ELISA检测结果存在较大差异,与各实验室所用试剂盒有很大关系,如果以后遇到在其他实验室有过类似检测的,我们一定要重视,可能在你的实验室就无法检测出来。对处于检测灰区的标本,结果判断应慎重,有条件的应进行重复测定或者进行核酸扩增试验再出报告<4>。对于特殊的高危人群需进一步随访,定期复查。在做ELISA时只有采用正确的方法,而且在做实验时可以考虑温度的原因,适当的延长孵育显色的时间,可以使颜色变深,因为样本A值越小,CV值就越大<5>,重复性就不好。实验时一定不能把两步法的试剂盒改成一步法用,这样实验多半失败,同时还可能造成假阴性结果,从网上查到的资料,一般的乙肝表面抗原定量检测值大于0.18ng/ml时,就说明该患者体内的乙肝表面抗原为阳性结果,反之被以为是乙肝表面抗原阴性。如果两步法改成了一步法用,那么稀释的溶液不但与一抗的结合机会变少了,抗体过量出现了前带现象,而且还可能与二抗结合后不与一抗结合,而且一步法中使用的是单抗,抗体的浓度也是厂家反复验证的出来的,这都是值得注意的问题。同时,本实验中还存在一个缺陷,该试剂盒是用来检查临床标本(血清)的,而我们要验证的也是该方法对临床乙肝表面抗原定量检测的准确度和精密度,而实验时所采用的的无论是标准品还是质控品都是用的PBS缓冲液来稀释的,其实如果这个实验要严谨的话一定要用乙肝表面抗原阴性的血清来(生物基质)做实验,可以先有PBS配制成高浓的的HBsAg液之后在用,阴性血清来稀释成我们的标准品和质控品,因为样本OD值越小,CV值就越大,血清中某些物质在反应中可能起到一些作用,对提高整体的OD值有一定的作用。实验中,震荡作用绝对不能免去,标本在振荡情况下测定的OD值均高于标本在没有振荡情况下测定的OD值,这说明振荡对检测结果影响较大。
3.4 ELISA中可能存在的假阴性结果分析
检测时过量的HBsAg分别与固相载体和酶标抗体结合,不再形成夹心复合物而呈现钩状反应。ELISA一步法操作简便,但由于使用单克隆抗体,由此也可能出现假阴性结果,所以不能把显色板的显色深浅与病毒含量或HBsAg量等同,两者不成正比关系,显色深者只表示包被的抗体与受检抗原最大限度地形成了夹心复合物;而显色浅者一部分除量低外,还有一部分是过量的标本,血清经稀释后呈不同程度阳性说明这一点。<7>除此之外可能的原因还有,试剂和板从试剂盒内取出,室温平衡时间太短。质控品溶解后室温平衡不充分,加样前没有振摇混匀。显色剂滴量不足或顺序颠倒。37℃温箱孵育时间不够。说明书上37℃ 孵育30 min应理解为:加液完毕放在37℃ 温箱中的时间40 min,其中前10rain为达到37℃孵育平衡所需时间。另外还有:花板:多半是洗板不净的原因,可检查洗板机程序的洗涤次数、静置时间是否准确;洗板过程中是否有窜液现象。重复性不好:酶标仪滤光片不对或输入波长不对,不同批号试剂盒中组分混用,尤其是显色剂B;存在板间差异,可作多孔复试。阳性对照太低:阳性对照或试剂盒平衡时间不够,且应充分混匀;酶结合物活性下降;可能洗板次数超过5次。本底较高酶标仪只用单波长读数,没有消除空白本底,应该用450/630 nm双波长读数;洗板机吸头吸液不干净,或溢流而交叉污染;加酶时加到孔壁上;血清溶血。
结论
通过对HBsAg的回收率,批内重复性、批间重复性、检出限的评价和分析,证实该检测系统的性能能够满足临床定量检查HBsAg的试剂盒其准确性和精密度均满足需求。为保证实验结果的准确可靠,首先应选用高质量、高精密度的试剂盒。实验的操作水平会影响到实验的精密度和准确性,应用全自动酶免分析系统可以提高实验的精密度和准确性,从而保证检测结果的可靠性,同时,精密度和准确性的高低可能影响实验结果的判定,对于灰区标本应进行重复测定,以免造成误检。
参考文献:
<1>. 张建荣 席向红 郭小龙 崔 洁《电化学发光法测定乙肝表面抗原的方法学性能评价》 华北煤炭医学院学报2011年7月第l3卷第4期J North China Coal Medical University 2011 July,13(4) .
<2>. 金海甲 ,刘 杰 ,崔秉玉 ,陈百艳 ,刘德新《ELISA方法检测尿液slgA的方法学评价》北华大学学报{自然科学版)第2卷第5期 文章编号:1009 4822.
<3>. 李岩 姜梅 陈松楠 李娜 《金标法与酶联免疫吸附法检测乙肝表面抗原的方法学比较》 中国疗养医学2010年4月第19卷第4期.
<4>. 吴先玉《1例乙肝表面抗原低浓度水平检测的分析》中外医学研究 2010年8月 第8卷第17 .
<5>. 李红 新李俊 武聂 希会 李友根《酶免法检测乙肝表面抗原实验精密度研究》.
<6>. 张凤莲 施岳雨 孙淑莉 《乙肝表面抗原单项阳性结果必须做乙肝五项检测》文章编号:1008—0899(2003)03—0051—02.
<7>. 冯 岭(江苏省中医院检验科江苏 南京210029)《乙肝表面抗原假阴性结果的分析》 .
<8>. 唐 寅 《ELISA法测定HBsAg时质控品结果为阴性的原因分析及对策》 文章编号:1672—9455(2011)ll 1407—02 .
<9>. 郭种,张真铭《ELISA法检测HBsAg实验条件的优化》 文章编号:1673~4130(2011)06—0656-02 .





