
Flowering Locus C(FLC)是开花抑制基因,编码 MADS-box 转录因子(Michaels & Amasino,1999),广泛存在于拟南芥、芥菜、甘蓝、大白菜和油菜等十字花科作物中。FLC 在转基因植物中过量表达,会抑制开花。例如油菜 BnFLC 在拟南芥中表达能延迟开花 3 周至 7 个月,拟南芥 AtFLC在油菜中表达能延迟开花 2 周至 6 周(Sanda & Amasino,1996;Tadege et al.,2001);拟南芥 AtFLC在烟草中表达可延迟开花约 14 d(Hassan et al.,2005);甘蓝 BoFLC3在芥菜中表达可延迟开花约 9d(杨海鹏 等,2013)。目前,利用酵母双杂、凝胶阻滞和免疫共沉淀等方法对 FLC 抑制开花的分子机理进行了深入研究,发现拟南芥 FLC 基因编码的蛋白能够与另一个开花抑制因子 SHORTVEGETATIVE PHASE(SVP)相互作用,并结合到开花信号整合子基因 FT 和 SOC1 的 CArG 基序,抑制 FT 和 SOC1 的表达,从而阻止茎端分生组织向开花转变(Fujiwara et al.,2008;Li et al.,2008;Jung & Müller,2009)。在芥菜作物中,利用 pET 原核表达系统和酵母真核表达系统也证实了芥菜FLC 家族成员 FLC2能够与 SVP 蛋白互作(汤青林 等,2011,2012)。
FLC 属于一个多基因家族。Li 等(2005)以大白菜 BrFLC 的编码序列制作探针进行 Southern杂交,发现了多条杂交信号,证实了 FLC 基因确实为多基因家族。目前在大白菜中发现有 4 个 FLC家族成员(Schranz et al.,2002;Wu et al.,2012),其中已证实 BrFLC1和 BrFLC2是主要的开花时间和春化反应基因(Yuan et al.,2009;Zhao et al.,2010;Wu et al.,2012)。另外,在油菜中也克隆了 5 个 FLC 家族成员(Tadege et al.,2001),均能抑制开花。此外,Zou 等(2012)从 3 份油菜材料中共获得了 9 个 FLC 同源基因(4 个来源于 A 基因组,5 个来源于 C 基因组),并得到与开花时间相关的 4 个 QTL。
虽然种子春化作物大白菜、油菜、芥菜和拟南芥 FLC 家族基因已有相关研究,但是典型绿体春化作物甘蓝 FLC 家族成员的研究非常少,它们调控开花时间的分子机制也未见深入研究和报道。尽管目前已证实甘蓝 FLC3成员能够与开花抑制因子 SVP 相互作用(杨朴丽 等,2013),但甘蓝 FLC家族其他成员是否也可发生类似作用,它们在蛋白作用强度上有何差异,这一作用差异对开花时间又有何影响,目前还未得到确切的分子证据。
本试验中从甘蓝中克隆多个 FLC 同源基因,构建猎物质粒,酵母双杂交并结合点突变分析 FLC的氨基酸变异对 FLC/SVP 聚合化的影响,为进一步获得转基因 FLC 的定点突变体、体内敲除或增补 FLC 家族成员、FLC/SVP 聚合强度的活体鉴定及其开花时间分子调控等奠定基础。
1、 材料与方法
1.1 材料
甘蓝材料‘ZQ-67’为‘早秋–67’母本系,由重庆市蔬菜学重点实验室提供。酵母双杂交系统(Matchmaker Gold Yeast Two-Hybrid System)、Aureobasidin A(以下简称 AbA)、X-a-Gal、YPD、YPDA 及各种酵母缺陷型培养基均购自 Clontech 公司。EcoRⅠ、BamHⅠ和 PstⅠ限制性内切酶购自TaKaRa 公司。pEASY-Blunt Simple Cloning Vector 克隆载体、DNA 回收纯化试剂盒、质粒提取试剂盒购自 TransGen 公司。高保真 DNA 聚合酶购自 Invitrogen 公司。高效连接酶购自 ToYoBo 公司。
1.2 BoFLC 家族基因及 BoSVP 的克隆
根据大白菜基因组序列(Wang et al.,2011)、拟南芥 AtFLC(NCBI 登录号 AY850000)和油菜BnFLC1~ BnFLC5(NCBI 登录号分别为 AY036888、AY036889、AY036890、AY036891、AY036892)设计甘蓝 BoFLC 家族基因(记作 BoFLCy1~ BoFLCy5)的上、下游引物;以拟南芥和白菜 SVP 基因序列(NCBI 登录号分别为 AF211171、AY356366)设计甘蓝 BoSVP 的引物(表 1)。

提取甘蓝茎尖 RNA,反转录 cDNA 后以此为模板,采用高保真聚合酶 PCR 扩增,分别以 FF(E)1/FR(Ps)、FF(E)2/ FR(Ps)、FF(E)3/ FR(Ps)、FF(E)4/ FR(Ps)、FF(E)5/ FR(Ps)为引物组合克隆甘蓝BoFLCy1、BoFLCy2、BoFLCy3、BoFLCy4、BoFLCy5;以 S(E)/S(B)为引物组合克隆甘蓝 BoSVP。
为删除 MIKC 蛋白 BoFLCy1~ BoFLCy5的 MADS 域,重新设计上游引物(表 1)。以 FF(E)124/FR(Ps)为引物组合分别从 BoFLCy1、BoFLCy2、BoFLCy4亚克隆 BoFLC▲y1、BoFLC▲y2、BoFLC▲y4;以 FF(E)35/ FR(Ps)为引物组合分别从 BoFLCy3、BoFLCy5亚克隆 BoFLC▲y3、BoFLC▲y5。
1.3 酵母重组表达载体构建
将 BoFLCy1~ BoFLCy5、BoFLC▲y1~ BoFLC▲y5质粒经 EcoRⅠ/PstⅠ双酶切后,连接到酵母载体pGBKT7,分别构建酵母重组质粒 pGBKT7-BoFLCy1~ pGBKT7-BoFLCy5和 pGBKT7-BoFLC▲y1~pGBKT7-BoFLC▲5。将 BoSVP 质粒经 EcoRⅠ/BamHⅠ双酶切后,连接到酵母载体 pGADT7,构建重组质粒 pGADT7-BoSVP。将 EcoRⅠ/PstⅠ、EcoRⅠ/BamHⅠ双酶切鉴定为阳性的酵母重组质粒送样测序。
1.4 酵母感受态制备、转化及自激活与毒性检测
参考 Clontech 公司 Gold Yeast Two-Hybrid System 操作手册,从 YPDA 固体培养基上挑选直径为 2 ~ 3 mm 的 Y187 和 Y2HGold 酵母单菌落,分别制备酵母感受态细胞。采用醋酸锂转化法,将重组质粒pGBKT7-BoFLCy1~ pGBKT7-BoFLCy5和pGBKT7-BoFLC▲y1~ pGBKT7-BoFLC▲y5分别转入 Y2HGold 感受态细胞;将 pGADT7-BoSVP 转入 Y187 感受态细胞。
将酵母转化子 Y2HGold[pGBKT7-BoFLCy1] ~ Y2HGold[pGBKT7-BoFLCy5]、Y2HGold[pGBKT7- BoFLC▲y1]~ Y2HGold[pGBKT7-BoFLC▲y5]分别涂在 SD/-Trp、SD/-Trp/X-a-Gal、SD/-Leu/-Trp ( 以 下 简 称 DDO ) 和 SD/-Trp/X-a-Gal/AbA 固 体 平 板 上 ; 将 转 化 子 Y187[pGADT7-BoSVP]涂在 SD/-Leu、SD/-Leu/X-a-Gal、SD/-Leu/-Trp 和 SD/-Leu/X-a-Gal/AbA 固体平板上。以空载体转化子 Y2HGold[pGBKT7]和 Y187[pGADT7]为阴性对照,并以酵母双杂交系统自带的 Y2HGold[pGBKT7-Lam]× Y187[pGADT7-T]为阴性对照,Y2HGold[pGBKT7-53]×Y187[pGADT7-T]为阳性对照。30 ℃培养 3 ~ 5 d,进行自激活和毒性检测。
1.5 酵母双杂交及其蛋白互作检测
从酵母菌 Y187、Y2HGold 转化子中分别挑取单个阳性克隆于 500 μL 2 × YPDA 中混匀,30 ℃培养 20 ~ 24 h,取适量涂于 SD/-Trp、SD/-Leu 和 DDO 固体培养基,30 ℃倒置培养 3 ~ 5 d 至阳性克隆出现。再从DDO固体培养基上挑取阳性克隆分别涂于SD/-Leu/-Trp/AbA(以下简称DDO/AbA)、SD/-Ade/-His/-Leu/-Tr(p以下简称 QDO)和 SD/-Ade/-His/-Leu/-Trp/X-a-Gal/AbA(以下简称 QDO/X-α-Gal/ AbA)固体培养基,30 ℃培养 3 ~ 5 d 观察是否有蓝色菌落。
1.6 突变体构建及其相互作用
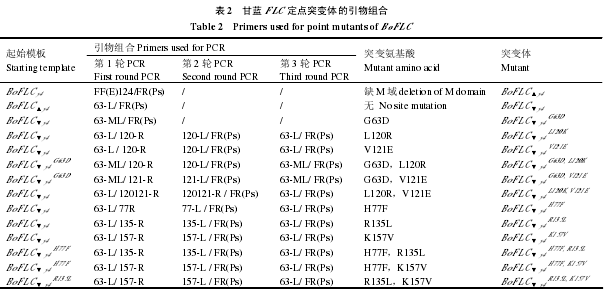
DNAstar 软件预测 BoFLCy4蛋白的二级结构,并在线(http://web.expasy.org/protscale/)分析编码氨基酸的疏(亲)水特性,设计点突变引物 14 条(表 1)。利用重叠延伸 PCR 技术共进行 3 轮次PCR(表 2),分别将第 63、120 和 121 位的疏水氨基酸突变为亲水氨基酸,将第 77、135 和 157 位亲水氨基酸突变为疏水氨基酸,共构建 6 个单突变体和 6 个双突变体(表 2)。在突变体构建时,先分别将第 1、2 轮次的 PCR 产物电泳,回收目的条带;再等量混合使其互为模板及引物,加入 dNTP 及Pfu 酶在 PCR 仪上扩增 10 个循环;并以此次的产物作为第 3 轮次 PCR 的模板,克隆突变体并测序验证,连接到酵母载体 pGBKT7 后转化酵母菌 Y2HGold,与 BoSVP 酵母双杂交。
1.7 β–半乳糖苷酶活性测定
采用 Thermo 公司 Yeast β-Galactosidase Assay Kit 试剂盒,按照其操作方法测定酵母融合菌的OD660值和 A420吸光值,每样品重复测 3 次,取平均值,计算 β–半乳糖苷酶活性。β–半乳糖苷酶活性 =(1 000 ×A420)(/t × V × OD660)。t 为反应时间(min),V 为用作检测活性的菌悬液体积(mL),活性单位表示为‘Miller Units’(汤青林 等,2013)。
2、 结果与分析
2.1 BoFLC 家族基因克隆及氨基酸序列分析
克隆的甘蓝 BoFLCy1~ BoFLCy5基因分别为 607、607、604、607 和 604 bp,均含完整编码区(NCBI登录号 KF797913 ~ KF797917)。Blast 在线分析表明:BoFLCy1、BoFLCy2、BoFLCy4基因序列之间有 6 个(cDNA 序列的 5′ 端 2 个,中部 1 个,3端 3 个)碱基差异,它们与油菜 BnFLC3(登录号AY036980)同源性高达 98%。而 BoFLCy3与 BoFLCy5基因序列之间有 5 个(cDNA 序列 5′ 端 4 个,3′ 端 1 个)碱基差异,它们与油菜 BnFLC4(登录号 AY036981)同源性高达 99%。这表明已克隆到甘蓝 FLC 同源基因。为准确分析 BoFLCy1~ BoFLCy5(含起始密码 ATG 之前的 9 个碱基)融入酵母载体后的作用差异,将该非编码区也翻译成了 3 个氨基酸(图 1,★所示)。
结构域分析表明(图 1):BoFLCy1~ BoFLCy5均属 MIKC 型蛋白,含 M、I、K 和 C 域。M 域完全相同,均含 50 个氨基酸。但 BoFLCy1、BoFLCy2、BoFLCy4的 IKC域与 BoFLCy3、BoFLCy5存在差异。BoFLCy1、BoFLCy2与 BoFLCy4的 I、K 和 C 域均分别为 25、81 和 33 个氨基酸;而 BoFLCy3与 BoFLCy5的 I、K 和 C 域则分别为 19、87 和 32 个氨基酸。
BoFLCy1、BoFLCy2与BoFLCy4蛋白I域完全相同;但K域在第151位氨基酸上存在差异,BoFLCy1为缬氨酸 V,而 BoFLCy2和 BoFLCy4均为谷氨酸 E。另外,BoFLCy1与 BoFLCy2蛋白 C 域末端有 1个位点不同,前者为酪氨酸 Y,后者为天冬酰胺 N;BoFLCy1与 BoFLCy4的 C 域也有 1 个位点不同,前者为脯氨酸 P,后者为精氨酸 R(图 1,● 所示)。此外,BoFLCy3与 BoFLCy5蛋白的 I 域、K 域均完全相同,但 C 端域存在 1 个位点差异:前者为脯氨酸 P,后者为精氨酸 R(图 1,● 所示)。
信号肽预测表明:BoFLCy1~ BoFLCy5蛋白的 N 端均不含信号肽,不属于胞外分泌蛋白或膜蛋白,在酵母双杂交检测蛋白相互作用时,不会受到信号肽的干扰。
2.2 BoFLC 家族蛋白的进化树分析
为进一步分析甘蓝 FLC 家族蛋白 BoFLCy1~ BoFLCy5的进化关系,从 NCBI 中搜索了油菜、大白菜等十字花科作物 FLC 家族蛋白的氨基酸序列,以 Clustalx2 软件进行比对,并通过 MEGA5 构建系统进化树(图 2)。本试验中所获得的 BoFLCy3、BoFLCy5蛋白与油菜 BnFLC4(登录号 AY036891)亲缘关系最近。

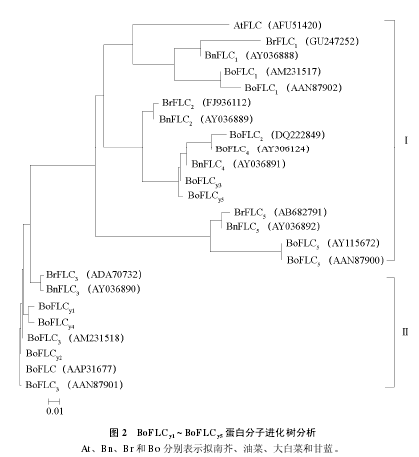
BoFLCy1、BoFLCy2、BoFLCy4蛋白与油菜 BnFLC3(登录号 AY036890)、大白菜 BrFLC3(登录号 ADA70732)、甘蓝 BoFLC3(登录号 AM231518)亲缘关系最近。根据 FLC 同源蛋白的进化关系,可将其分成两类:甘蓝 BoFLCy3、BoFLCy5属于第Ⅰ类;甘蓝 BoFLCy1、BoFLCy2、BoFLCy4属于第Ⅱ类。第Ⅰ类与第Ⅱ类之间的亲缘关系较远(图 2)。
2.3 酵母重组表达质粒构建与鉴定
将甘蓝 BoFLCy1~ BoFLCy5分别构建到 pGBKT7,获得的猎物质粒 pGBKT7-BoFLCy1~pGBKT7-BoFLCy5分别经 PCR 检测、EcoRⅠ/PstⅠ双酶切鉴定(图 3,A)及测序表明:目的基因的核苷酸序列、插入载体位置与方向均完全正确,且无移码突变。重组质粒 pGBKT7-BoFLCy1~pGBKT7-BoFLCy5分别转化 Y2HGold 后,能在 SD/-Trp/X-α-Gal 平板长出白色菌落,且与对照Y2HGold[pGBKT7]菌落大小相当。但是在 SD/-Trp/X-α-Gal/AbA 上不能生长,也不能在 SD/-Leu/-Trp上生长。说明 BoFLCy1~ BoFLCy5无自激活和毒性。
甘蓝 BoSVP 与酵母质粒 pGADT7 重组融合成 pGADT7-BoSVP,经过 PCR 检测、EcoRⅠ/ BamHⅠ双酶切鉴定(图 3,A)及测序,表明该酵母融合载体也构建正确。pGADT7-BoSVP 转化酵母菌 Y187后能在 SD/-Leu/X-α-Gal 平板上长出白色菌落,与对照 Y187[pGADT7]菌落大小相当。但在SD/-Leu/X-α-Gal/AbA 和 SD/-Leu/-Trp 上均不能生长,也无自激活和毒性现象。
此外,删掉 BoFLCy1~ BoFLCy5的 MADS 域,获得含 IKC 域的截短体 BoFLC▲y1~ BoFLCy▲5,分别构建酵母重组质粒 pGBKT7-BoFLC▲y1~ pGBKT7-BoFLC▲5,并经过 EcoRⅠ/ PstⅠ双酶切(图 3,B)及测序验证后,转化酵母菌 Y2HGold、Y187,也无毒性和自激活现象。

2.4 BoFLC 家族蛋白与 BoSVP 相互作用
图 4 表明:除了阳性对照(P)能够在 QDO/X-α-Gal/ AbA 平板长出蓝色菌落外,所有阴性对照(N、F1 ~ F5、MF1 ~ MF5)均不能生长,表明本酵母双杂交系统严谨可靠。Y2HGold[pGBKT7-BoFLCy1]~ Y2HGold[pGBKT7-BoFLCy3]、Y2HGold[pGBKT7-BoFLCy5]分别与 Y187[pGADT7-BoSVP]融合后,涂布在 DDO 平板上长出白色菌落,能形成二倍体酵母菌。
融合菌依次经 DDO/AbA、QDO 平板筛选后,涂布在 QDO/X-α-Gal/AbA 平板,长出了蓝色菌落,表明同时激活了酵母的报告基因 HIS3、AUR1-C、ADE2 和 MEL1,证明 BoFLCy1~ BoFLCy3、BoFLCy5能够与 BoSVP 相互作用(图 4,H1、H2、H3 和 H5)。但是,Y2HGold[pGBKT7-BoFLCy4]与 Y187[pGADT7-BoSVP]融合后不能在 QDO/X-α-Gal/AbA 平板上生长(图 4,H4),说明构建到酵母载体上的 BoFLCy4融合子(含起始密码之前的 3 个氨基酸 TET)不能与 BoSVP 相互作用。
删除 M 域、仅保留 IKC 域的截短体 BoFLC▲y1~ BoFLC▲y5与 BoSVP 酵母双杂交表明:Y2HGold[pGBKT7-BoFLC▲y1]~ Y2HGold[pGBKT7-BoFLC▲y5]与 Y187[pGADT7-BoSVP]均可融合,并能在 QDO/X-α-Gal/AbA 上长蓝色菌落(图 4,MH1 ~ MH5),激活酵母 4 个报告基因 HIS3、AUR1-C、ADE2 和 MEL1。说明去掉 M 域的 BoFLC▲y1~ BoFLC▲y5均能与 BoSVP 相互作用。
BoFLCy4氨基酸序列与BoFLCy1、BoFLCy2高度相似,其M域完全相同。但融入酵母载体pGBKT7后,紧邻起始密码子的 9 个非编码碱基也翻译成了 3 个氨基酸,为 TET(图 1,★ 所示),使得 BoFLCy4融合子(BoFLCy4蛋白的 N 端插入 TET)不能与 BoSVP 相互作用,但 BoFLCy1、BoFLCy2以及截短体 BoFLC▲y1、BoFLC▲y2、BoFLC▲y4均可与 BoSVP 相互作用。由此推测:BoFLCy4蛋白较为敏感,当 N 端插入 3 个氨基酸 TET 后阻止了它与 BoSVP 的聚合。
综上所述,甘蓝的 BoFLC 家族蛋白均可与 BoSVP 相互作用。
2.5 BoFLC 变异位点对 FLC/SVP 聚合化的影响
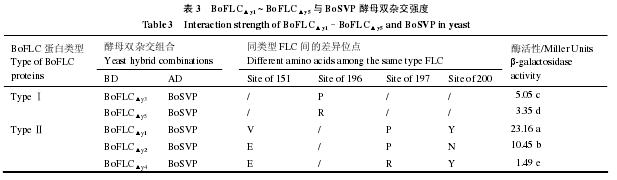
BoFLC▲y1~ BoFLC▲y5对 FLC/SVP 聚合强度存在显著差异(表 3):BoFLCy1> BoFLCy2>BoFLCy3> BoFLCy5> BoFLCy4。第Ⅱ类蛋白 BoFLC▲y1、BoFLC▲y2和 BoFLC▲y4平均聚合强度(β–半乳糖苷酶平均活性为 11.7)高于Ⅰ第类 BoFLC▲y3、BoFLC▲y5的平均强度(酶活为 4.2)。但是,作用最强的 BoFLC▲y1(酶活性为 23.16)和最弱的 BoFLC▲y4(酶活性为 1.49)均出现在第Ⅱ类。
在第Ⅰ类中,BoFLC▲y3蛋白第 196 位的疏水性脯氨酸 P 变异为亲水性精氨酸 R 后(位于 C 端域),即为 BoFLC▲y5,其作用强度会显著减弱(酶活性由 5.05 变为 3.35),降为 66.34%。在第Ⅱ类中,作用强度为:BoFLC▲y1> BoFLC▲y2> BoFLC▲y4。当 BoFLC▲y1第 151、200 位氨基酸同时变异(即 BoFLC▲y1V151E和 BoFLC▲y1Y200N),则为 BoFLC▲y2,作用强度(酶活性)由 23.16降为 10.45,降到 45.12%。当 BoFLC▲y2第 197、200 位同时变异(即 BoFLC▲y2P151R和 BoFLC▲y2N200Y),则为 BoFLC▲y4,作用强度(酶活性)降为 12.26%。当 BoFLC▲y1第 151、197 位同时变异(即BoFLC▲y1V151E和 BoFLC▲y1P197R),则为 BoFLC▲y4,作用强度(酶活性)急剧减弱,降为 6.43%。

以上第Ⅰ、Ⅱ类 FLC 家族蛋白第 151、196、197 和 200 位点的疏水氨基酸变异为亲水氨基酸后,均会明显减弱 FLC 与 SVP 的作用,说明该变异位点为疏水氨基酸有利于 FLC/SVP 聚合。
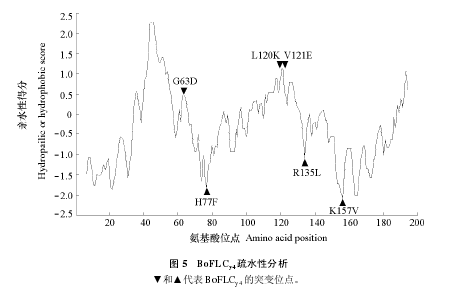
2.6 BoFLC 保守位点突变对 FLC/SVP 聚合化的影响
为进一步研究 FLC 保守位点的疏水氨基酸是否也对 FLC/SVP 聚合化有影响,选择甘蓝 FLC 家族中作用最为敏感且强度最弱的 BoFLCy4,根据蛋白疏水特性和图谱的波谷或波峰,在 IK 域内各筛选了 3 个亲(疏)水氨基酸位点进行突变研究(图 5)。这些位点在甘蓝、芥菜、白菜、拟南芥等FLC 家族蛋白中高度保守,属于非变异性位点。其中第 77(I 域内,组氨酸 H)、135 和 157 位(K域内,精氨酸 R 和赖氨酸 K)为亲水位点,分别突变为苯丙氨酸 F、亮氨酸 L 和缬氨酸 V。而第 63(I 域内,甘氨酸 G)、120 和 121 位(K 域内,亮氨酸 L 和缬氨酸 V)为疏水位点,分别突变为天冬氨酸 D、赖氨酸 K 和谷氨酸 E(图 5)。
BoFLCy4的 K 域有 3 个 α 螺旋和 1 个 β 折叠(图 6),其中第 1 和第 3 个 α 螺旋分别延伸到 I域和 C 域。突变位点 120、121、135、157 均位于 K 域的第 3 个 α 螺旋中(在 K 域内)。此外,该蛋白的 I 域有 2 个 β 折叠,突变位点 63 位于 I 域的第 1 个 β 折叠中,而突变位点 77 位于第 1 个 α螺旋的延伸区域(在 I 域内)。以上位点突变后均不会破坏蛋白的 α 螺旋和 β 折叠。
先以 BoFLCy4作为起始模板,FF(E)124/ FR(Ps)为引物亚克隆截短体 BoFLC▲y4。再以 BoFLC▲y4为模板,63-L/FR(Ps)为引物进一步亚克隆,记作 BoFLC▼y4或 BoFLC▼y4WT(与之前的截短体BoFLC▲y4相区别)。并在 BoFLC▼y4基础之上将疏水位点(第 63、120、121 位)或者亲水位点(第77、135、157 位)分别单突变和双突变,共构建 12 个突变体(表 2),与 BoSVP 酵母杂交并测定β–半乳糖苷酶活性。

与 BoFLC▼y4WT× BoSVPWT酵母双杂交组合(酶活性为 1.49)相比,发生在 I 域的 2 个单突变体 BoFLC▼y4H77F、BoFLC▼y4G63D中,不论第 77 位亲水 His 突变为疏水 Phe(酶活性为 1.51),还是第 63 位疏水 Gly 突变为亲水 Asp(酶活性为 1.41),作用强度均不会发生显著变化,说明 FLC/SVP聚合强度不由 I 域中该氨基酸的亲(疏)水性调节。
在 K 域的 4 个单突变体 BoFLC▼y4R135L、BoFLC▼y4K157V、BoFLC▼y4L120K和 BoFLC▼y4V121E中,第 135 位亲水 Arg 突变为疏水 Leu,或者第 157 位亲水 Lys 突变为疏水 Val 后,作用强度均增加(酶活性分别为 4.36 和 1.84),但 BoFLC▼y4R135L显著高于 BoFLC▼y4K157V,而第 120 位疏水 Leu 突变为亲水 Lys,或者第 121 位疏水 Val 突变为 Glu 后,均会显著减弱(酶活性分别为 0.82 和 0.63),说明K 域中该位点的亲(疏)水特性能调节 FLC/SVP 聚合化。
在亲水氨基酸突变为疏水性的双突变体 BoFLC▼y4H77F, R135L、BoFLC▼y4H77F, K157V、BoFLC▼y4R135L, K157V中,作用强度均显著增强(酶活性分别为 4.51、1.80 和 5.73),其中 BoFLC▼y4R135L, K157V最强,该双突变位点(第 135、157 位)均位于 K 域,然而在疏水氨基酸突变为亲水性的 BoFLC▼y4G63D, L120K、BoFLC▼y4G63D, V121E和 BoFLC▼y4L120K, V121E中作用强度均显著减弱(酶活性分别为 0.78、0.52 和 0.15),但 BoFLC▼y4L120K, V121E最弱,该双突变位点(第 120、121 位)也位于 K 域,说明 K 域亲(疏)水特性对调节 FLC/SVP 聚合强度有较大贡献。
3、 讨论
3.1 FLC 基因在芸薹属作物中有多个家族成员
Tadege 等(2001)以拟南芥开花抑制基因 AtFLC 为探针,从油菜 cDNA 文库中克隆了 5 个 FLC基因,发现油菜(为 AACC 基因组)的 FLC 基因为多基因家族,其编码蛋白 N 端具有高度保守的MADS 域,将油菜 5 个 FLC 基因转入拟南芥后均可延迟开花时间。本研究中从甘蓝中也克隆了 5个 FLC 基因,且编码 5 个不同的蛋白,并根据分子进化分成了 2 类,不同类的家族成员之间相差 1个氨基酸,说明甘蓝(为 CC 基因组)的 FLC 也为多基因家族。本实验室在芥菜(为 AABB 基因组)中也克隆到了 5 个不同的 FLC 基因,也编码不同的蛋白,说明芥菜 FLC 也为多基因家族。另外,在 AA 基因组代表作物大白菜中,只发现了 4 个 FLC 家族基因,而在拟南芥中 FLC 仅有 1 个拷贝(Schranz et al.,2002;Wu et al.,2012)。由此表明:在十字花科植物中,拟南芥属的拟南芥 FLC为单基因;而芸薹属作物油菜、甘蓝、芥菜、大白菜的 FLC 为多基因家族,但即便均为芸薹属,基因组类型不同其 FLC 家族成员的数量也并不完全相同。FLC 家族成员的数量和功能是否与 AA(白菜)、BB(黑芥)、CC(甘蓝)、AABB(芥菜)、AACC(油菜)等基因组的不同类型有关,还有待深入研究。另外,本实验室杨海鹏等(2013)将甘蓝 FLC 家族成员之一的 BoFLC3转入芥菜后,能延迟开花,说明至少 BoFLC3可调节开花时间。本试验克隆的 5 个 BoFLC 成员中,有 3 个(BoFLCy1、BoFLCy2和 BoFLCy4)与 BoFLC3的编码氨基酸在分子进化上同属第Ⅱ类(图 2),推测这 3 个成员也能够调节开花时间,但调节强度可能存在差异。而另 2 个成员 BoFLCy3和 BoFLCy5是否具有类似的功能,还缺乏分子证据。因此,要正确理解 BoFLC 家族成员功能的协同性和差异性,还需进行植物体内蛋白相互作用及其转基因功能验证。
3.2 FLC 蛋白疏水氨基酸位点变异影响 FLC/SVP 聚合
拟南芥单拷贝的 FLC 基因能抑制开花时间,其编码蛋白能够与开花抑制因子 SVP 形成蛋白聚合体(Li et al.,2008)。本研究中甘蓝 5 个 FLC 基因的编码蛋白也均能够与 SVP 结合成蛋白复合体,激活酵母报告基因 HIS3、AUR1-C、ADE2 和 MEL1,但其作用强度存在明显差异。FLC 蛋白的K 域内氨基酸的变异位点和保守位点均对作用强度有影响,其中疏水氨基酸可增加相互作用。Yang等(2003)在对拟南芥 AP3/PI 二聚化的研究发现,K 域的疏水氨基酸非常重要,能够控制 AP3/PI互作强度。这与本研究结果相似:甘蓝 FLC 蛋白第 135、157 位(K 域内)突变为疏水氨基酸后能促进 FLC/SVP 聚合;但第 120、121 位(K 域内)突变为亲水氨基酸后作用明显减弱。说明疏水氨基酸确实能够调节蛋白作用强度。另外,Yang 和 Jack(2004)对拟南芥 PI/SEP3 或 PI/SEP1 蛋白复合体研究发现,尽管 K 域保守的疏水氨基酸能增强该蛋白互作,但主要位于 K 域的第 1 和第 2 个 α螺旋内,K 域内第 3 个 α 螺旋中的疏水氨基酸不能调节该作用强度。而本研究结果与此并不完全相同,甘蓝 FLC 蛋白 K 域第 3 个 α 螺旋中的疏水氨基酸能够增强 FLC/SVP 二聚化。但是在 I 域中的第 63、77 位氨基酸亲(疏)水特性不会明显改变 FLC/SVP 聚合强度。说明甘蓝 FLC/SVP 聚合机制与拟南芥 PI/SEP3 或 PI/SEP1 存在差异,推测导致这一差异的原因可能是与蛋白空间构象及其相互作用区域有关。另外,影响 FLC/SVP 聚合强度的这些疏水氨基酸位点是否会改变甘蓝植株的花器官表型,它们对开花时间的影响究竟如何,还有待将这些突变体进行转基因功能验证。





