
高锰酸钾属于常见的通用型氧化剂[1 -2].因其氧化性能好、成本低、操作方便,且产生的副产物二氧化锰无毒无害[3],因而成为有机合成中常用的反应之一,在有机合成中占有重要的地位。高锰酸钾不易潮解,热稳定性好,能够氧化烯烃、炔烃、醇类、醛、芳香族化合物等有机物。但是由于其氧化反应一般在水体系中进行[4],而有机物大多不溶于水,因此使用 KMnO4水体系氧化有机物时产率较低[5],这成了 KMnO4氧化有机物反应应用的一大弊端。
随着化学实验技术的提高和有机合成者的不断探索,20 世纪 70 年代,相转移催化化学成了一项新的技术,逐渐应用到有机合成领域,KMnO4氧化有机物的研究有了突破性的进展。
例如有报道以苯基三甲基硫酸甲酯铵作相转移催化剂,以烯、醇和醛作为底物,能够很好地催化 KMnO4进行氧化反应[6].但相转移催剂大多结构复杂、合成工艺烦琐,价格昂贵,因此KMnO4在有机合成中的应用一直不是很理想。2008 年,我课题小组在无水丙酮有机体系中,用 KMnO4成功将棒状液晶醛类物质氧化为酸[7],使得 KMnO4在有机氧化方面的应用更加简单、且易操作。目前,有关高锰酸钾非水丙酮体系氧化反应方面的研究报道不是很多,特别是对于 KMnO4氧化简单有机化合物反应的影响因素有哪些,氧化性有多强,与有水体系中的氧化反应有什么不同之处等,缺乏相关报道,有必要详细研究。
1 实验部分
1. 1 仪器与药品试剂
MDSC Q100 差热扫描量热仪,美国 TA 公司,氮气保护,升 温 速 度 5 ℃ /min; IR Prestige 21 红 外 光 谱 仪,日 本SHIMADZU 公司,KBr 压片; GCMS QP2010 气 - 质联用仪,日本 SHIMADZU 公司,质谱条件: IE,70 eV.
高锰酸钾,苯甲醛,环己酮,苯甲醇等试剂均为国产分析纯。
1. 2 苯甲醛氧化制备苯甲酸
在干净的三颈烧瓶中加入一定量的 KMnO4固体,再加入一定量的丙酮,搅拌至 KMnO4固体完全溶解,再加入 3. 14 g1至室温,加入一定量的草酸至反应液的 pH 在 1 ~2 范围内,酸化一定时间后,将反应液转至分液漏斗中,加20 mL 乙醚萃取三次,合并萃取液并用水洗多次,将萃取液用旋转蒸发仪蒸发浓缩至干,得白色结晶,产品称重,计算产率。以气相色谱 -质谱联用仪、红外光谱仪、差热扫描量热仪对产品进行结构表征。
2 结果与讨论
2. 1 产物的结构表证
2. 1. 1 苯甲醛氧化产物的热性质表征
产品经 DSC 表征,结果见图1,目标产物的熔点为 122.2 ℃,苯甲酸的熔点为 122. 4 ℃( 文献值[8]) ,两者基本一致。
2. 1. 2 苯甲醛氧化产物的红外谱图解析
苯甲醛氧化产物红外光谱如图 2 所示,与纯苯甲酸的谱图一致。图中羧基上 O -H 的伸缩振动在 3000 ~2500 cm- 1; C = O的伸缩振动在 1690 cm- 1; 苯环的骨架振动在 1460 cm- 1,1500cm- 1; 单取代苯环上的 C - H 弯曲振动在 690 cm- 1,710 cm- 1.
2. 1. 3 氧化产物 GC / MS 分析结果
反应产物经过 GC/MS 检测,得到如图 3 所示的氧化产物总离子流图 A( TIC 图) 和质谱图 B( MS 图) .经过 GC/MS 系统软件和 NIST 147 质谱数据库检索分析可知,保留时间 5. 3 min的峰为苯甲酸峰( 质谱相似度 95%) ,产物纯度为 98. 4%.
2. 2 苯甲醛氧化制备苯甲酸的影响因素和最佳反应条件
2. 2. 1 溶剂用量对反应的影响溶剂( 丙酮) 的用量对实验有一定的影响。溶剂太少,KMnO4不能完全溶解,氧化会不彻底,产率受到影响; 溶剂太多,又造成不必要的浪费及环境危害。以苯甲醛与丙酮体积比为 1∶10,1∶20,1∶30,1∶40 的比例,按实验 1. 2 步骤反应,结果如表 1 所示。【1】
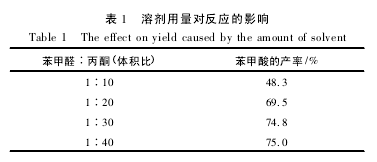
由表 1 可知,苯甲醛与丙酮的体积比为 1∶40,反应的产率最高,但是其产率升高仅比 1∶30 的情况多 0. 02%,而溶剂消耗比 1∶30 的情况多了 25%.综合考虑,1∶30 的条件较好。
2. 2. 2 酸化时间的影响初步试验表明,酸化时间是影响该氧化反应产率的一个重要因素,时间过短,酸化会不彻底,影响产品的收率。为了在较短的时间内得到最高的收率,特进行酸化时间对苯甲酸产率的影响实验。取酸化时间 0. 5 h,1 h,1. 5 h,按 1. 2 实验步骤进行,实验结果如表 2 所示。【2】

由表 2 可见,酸化时间在 0. 5 h 时,产率很低,1. 0 h 时,产率明显提高,1. 5 h 和 1. 0 h 的产率相差不是很大,考虑到反应效率,反应的酸化时间以 1. 0 h 为宜。
2. 2. 3 KMnO4用量对反应的影响【3】

在水体系中,KMnO4易自分解,通常要比计算量过量一倍以上反应才能进行完全。在有机溶剂丙酮体系中,可以克服KMnO4的自分解。初步研究显示,KMnO4的用量对产率的影响最大,需要进行详细的研究。为确保反应的产率,用量少会使氧化不完全,产率自然降低,用量过多会使产品的后处理比较麻烦。以反应物和 KMnO4的摩尔比分别为 1∶1、1∶1. 5、1∶2 为考察点,按 1. 2 实验步骤进行实验,实验结果如表 3 所示。
从表 3 中可以看出,KMnO4与反应物的摩尔比为 1∶2 时产率最高,但是高锰酸钾用量太大,对产品的外观有较大影响,而 1∶1. 5 反应条件的产率仅略低,所以选用 1∶1. 5 条件,且产品的后处理更容易。
2. 2. 4 最优条件下的实验结果以最优反应条件: 苯甲醛与丙酮的体积比为 1∶30,苯甲醛与 KMnO4的摩尔比为 1∶1. 5,酸化时间 1. 0 h,按 1. 2 实验步骤进行 3 次实验,结果见表 4.苯甲酸平均产率 92. 5%.【4】
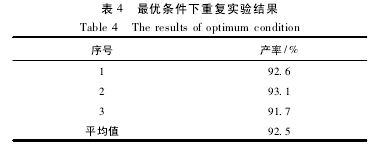
2. 3 无水、有水体系中 KMnO4氧化性强弱的对比采用上述实验步骤,在最优反应条件下,分别氧化环己酮、环己醇、苯甲醇。反应完后,通过 GC/MS 检测反应液。
通过对 GCMC 谱图的分析得知: 环己酮不能被氧化,环己醇和苯甲醇可以被部分氧化。在酸性水体系中上述物质能被高锰酸钾所氧化,说明在非水丙酮体系中,KMnO4的氧化性比酸性水体系中的氧化性弱。在无水体系中,KMnO4只能将醛或醇氧化,说明无水丙酮有机体系可以抑制高锰酸钾的氧化能力。
3 结 论
采用单因素实验法,对非水丙酮体系中高锰酸钾氧化苯甲醛的反应进行了研究。得到最优反应条件为: 以丙酮为溶剂,丙酮与苯甲醛的体积比为 1∶30,反应物和高锰酸钾的摩尔比为 1∶1. 5,反应温度为 57 ℃,反应时间 3 h,酸化时间 1. 5 h.
在产品的后处理中,通过在反应液中加入草酸,将剩余的KMnO4和反应后产生的 MNO2一起转化为二价锰离子,从而使反应溶液澄清,便于产品的萃取后处理。产物不需重结晶,即可得到纯度在 98%以上的产品。反应过程可避免 MNO2的吸附作用造成产物的流失。反应过程操作简单,产率较高。在有机溶剂无水丙酮中,KMnO4的氧化性比水体系中的氧化性弱,说明无水丙酮体系中可以控制高锰酸钾的氧化性。
参考文献
[1] 石鸿昌。有机化学中的氧化和还原[J].化学教育,2000( 4) :31 -34.
[2] 张占辉,刘庆彬。 分子碘催化的有机化学反应[J]. 化学进展,2006,18( 2) : 270 - 280.
[3] 杨晶晶,赵吉,马军。 不同还原剂对高锰酸钾氧化苯酚的影响[J].黑龙江大学自然科学学报,2013,30( 3) : 376 -380.
[4] 逯志昌,邱兆富,吕树光,等。 水相和泥浆系统中地下水成分对高锰酸钾氧化 TCE 的影响[J]. 环境工程学报,2012,6( 12) : 4529 -4534.
[5] 黄昌龙,王宏胜,李公春,等。 高锰酸钾氧化法制备 3,5 - 吡啶二甲酸[J]. 河北化工,2012,35( 5) : 44 -45.
[6] 李毅群,陈翠娟,周艳晖,等。 苯基三甲基硫酸甲酯铵催化高锰酸钾的氧化反应[J]. 暨南大学学报: 自然科学与医学版,1997,18( 5) :74 - 77.
[7] 郑敏燕,魏永生,安忠维。 选择氧化法合成烷基多环苯酰氧基苯甲酸的研究[J]. 有机化学,2008,28( 11) : 1948 -1953.





