
生理药动学(Physiologically based pharmaco kinetics,PBPK)模型是一种模拟机体循环系统的血液流向,将各器官或组织相互联结起来而建立的整体模型[1,2],利用该模型能够精确预测动物用药后各可食性组织中的药物浓度,制定合理的兽药残留休药期[3].目前,兽医领域的PBPK模型研究多集中在猪[3]、牛[4]、羊[5,6]及狗[7],家禽的相关研究较少。这主要是因为家禽种类很多,体型相对较小,生理学及解剖学参数不易获得,而且蛋鸡体内鸡蛋的形成过程极其复杂,不易用数学模型准确模拟。本文结合作者自身的研究经历,对PBPK模型在家禽体内的应用进行详细综述。
1 生理学及解剖学参数
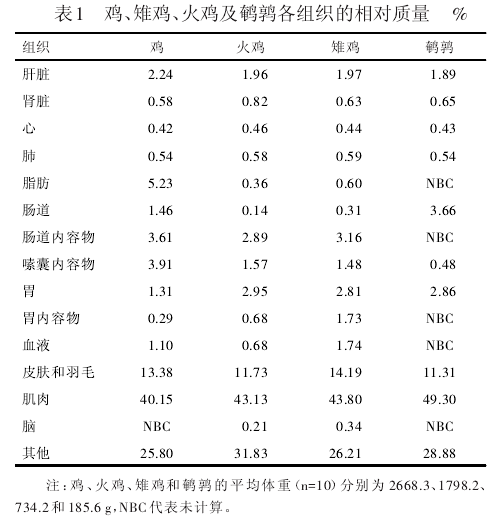
PBPK模型预测的准确性高,主要是因为该模型中包含了很多生理学和解剖学参数,如动物各组织的重量及各组织的血流速率常数等。相对于实验动物(小鼠、大鼠、家兔、恒河猴及比格犬等)[8]及其它家畜(猪和绵羊)[9]而言,目前尚无家禽生理学及解剖学参数的详细综述。Cortright等[10]分别解剖了10只鸡、雉鸡、火鸡和鹌鹑,获得了这四种禽体内各组织的重量,原文献报道的数值为绝对重量(单位为g),本文将其转换为体重百分数,列于表1中。除组织器官重以外,各组织的血流速率常数也是PBPK模型中的一类重要参数,该参数一般以心输出量的百分数来表示,而心输出量又可以用体重的幂函数来表示。以鸡为例,安静状态下其心输出量一般为200mL/kg·min,运动状态下则可高达293 mL/kg·min[11],一般流经肉鸡肝脏、肾脏、肌肉和脂肪的血流速率常数分别占心输出量的7%、10%、35%和2%左右[2].
2 肉鸡体内的PBPK模型
目前,肉鸡体内的PBPK模型相对较多。Cortright等[10]最先建立了单次静脉注射给药途径下咪达唑仑在肉鸡体内的PBPK模型,并将该模型外推至火鸡、雉鸡和鹌鹑,成功预测了咪达唑仑在四种禽体内的残留。Cortright等[10]所建模型由脂肪、肌肉、肾脏、肝脏、血浆及代表其他所有组织的其他室等6个隔室组成,咪达唑仑静脉注射后,直接进入血液循环,并分布到各组织中,其中到达肝脏和肾脏的药物分别经代谢和排泄消除,且代谢和排泄过程均符合一级速率特点。Cortright等[10]所建模型相对简单,因为模型中药物不存在吸收过程。但与哺乳动物相比,禽的消化道除了具有肠道外,还有嗉囊、腺胃和肌胃,这更增加了口服给药途径下禽体内PBPK模型建模的难度。
本课题组建立了马波沙星在肉鸡体内的PBPK群体模型[12],预测了多次灌胃给药后药物在肉鸡体内的残留休药期。模型中包含肺、肌肉、肾脏、肝脏、静脉血、动脉血、胃肠道内容物及其他组织等8个隔室。药物灌胃给药后,通过胃肠道吸收进入血液循环,并经肝脏代谢和肾脏排泄清除。
该模型中还考虑了马波沙星处置过程中的个体差异,将PBPK模型与蒙特卡洛模拟相结合,成功预测得到肉鸡连续3 d灌胃马波沙星(5 mg/kg·d)后的残留休药期为4 d.本课题组还建立了灌胃给药途径下氟苯尼考在肉鸡体内的PBPK模型,预测了氟苯尼考[2]及其残留标示物氟苯尼考胺[1]在肉鸡各可食性组织中的残留,并预测了多次灌胃后氟苯尼考的残留休药期[1].除口服给药外,肌内注射也是家禽养殖中常见的给药方式。鲍杰等[13]建立了肌内注射途径下土霉素在肉鸡体内的PBPK模型,并利用该模型预测了土霉素在鸡体内的药动学参数。其研究结果表明:土霉素在鸡体内吸收迅速,分布广泛,消除缓慢。鲍杰等所建模型是由Craigmill等[5] 所建的绵羊体内的PBPK模型外推而来,绵羊和鸡解剖学差异巨大,以往观点认为动物种属间差异较大时进行的外推一般较难获得较好的预测结果,但该研究证明PBPK模型在种间外推预测中具有较大优势。





