
�����ٿ��ⶾ�ڷ�Һ�����й�ũҵ��ѧԺ������������ҩ�о���������ũ����ѧԺ�������Ƶ���Զ������ж���ר����Ʒ,�ɽ�ĸ��¶���ǡ��������ơ�����þ��L-�����ǰ�һ���������,���α-��¶����ø�ĺϳɾ������õ��յ�����,����Ч����ɷ���ж�����Ķ������������ϰ�,��Ч����������������������ָ���[1].������ּ���о�С�����Զ��Ժ��Ǽ��Զ���,Ϊ���Ƽ��İ�ȫ�����ۺ��ٴ���ȫ������ɸѡ�ṩ����.
����1�����뷽��
����1.1�������
����1.1.1 ��Ҫ�Լ������� Sysmex F2820��ȫ�Զ�Ѫ���������(�ձ����ǹ�˾��Ʒ),�Ҵ�(AR).Ѫ��(GLUC),����YZB262-40-2010;�ܵ���(PROT),����A045-2;����(ALB),����A028-1;�ܵ��̴�(CHOL),����YZB0397-2012;�� �� �� �� (TBIL),�� ��C018;�� �� �� �� ø(AKP),����A059-2;����(Cr),����C011-1;���ص�(BUN),����C013-2;�Ȳ�ת��ø(AST),����C010-1.�Լ��о����Ͼ��������﹤���о����ṩ.
����1.1.2 ���鶯�P�������� SPF������״��������WistaС���������ݴ�ѧʵ�鶯�������ṩ,������Ϊ(17.6±1.0)g.���﷿��ʵ�����¶�Ϊ(24.0±1.0)��,���պڰ�ÿ12h����.����С����������ǰ�ڶ��﷿��Ӧһ��,����������,ÿ�ܸ�������3��,������ʳ��ˮ.
����1.2���鷽��1.2.1Ԥ����Ԥ����ǰ��С�������7dι���۲�,�۲�����С����������ˮ����ʳ,ÿ�տո�����������,��̭��Ȼ����С����.Ԥ��������ѡȡ40ֻС����,�����Ϊ5��,ÿ��8ֻ,���۸���,��200��400��800��1 600mg/kg����1���Թ�θ��ҩ,ȷ����ʽ����ļ�����Χ.
����1.2.2���Զ�����ʽ������ȡ20ֻС����,�����Ϊ2��.��ҩ�����������Ũ�� (1.0g/mL)������ݻ�(0.8mL)1���Թ�θ����ҩ��,�������õ����������ˮ,��ҩ�������۲�7d,�ⶨ����ҩ��.��ʽ����ʱ,��С���������Ϊ4��(�������3����ҩ��,��ҩ��ҩ�����ֱ�Ϊ3 200��1 600��800mg/kg),ÿ��10ֻ,���۸���,��40ֻ.��θǰ��6h��ʳ(������ˮ),���������ÿֻС����������������ҩ��,������θ��һ���Թ�θ��ҩ.������С�������ɲ�ʳ����ˮ.��ҩ��ÿ��۲�С����IJ�ʳ����ˮ������������ë���������,�����۲�7d.��ʱ��������С����,��¼�������,���ڵ�8���������С����������������,�۲츹ǻ��Һ�������ʵ�������ٵIJ����仯[2-7].
����1.2.3 �����Զ�������ȡС����80ֻ,�����Ϊ4��,ÿ��20ֻ,���۸���.��Ϊ�ߡ��С���3��������,��θ�����ֱ�Ϊ3 200��1 600��800mg/kg;������ÿ�ն�ʱ��θ����9g/L������ˮ.����������θ30d,ͣҩ���ٳ����۲�14d.
�����۲��ҩ�ڼ�С�����һ��״��,����С����һ�㽡������������۱��ж�С����Ľ���״��[8-9],��С������������,��ë���,�Դ̼�����,�Ի�������,���ж�Ϊ��;��ë��,ʧȥ����,С������Ȼ������Ծ,�ж�Ϊ��;��ë��������,���ֳɴ�,С�����پ�����Ծ,������������Բ�,������ʱ����ǿ����������,�ж�Ϊ��;С������������,����,�Ի���������,��ë���ҳɴ�,�ж�Ϊ����;С����Դ̼���Ӧ,��ë��ƿˢ״,վ������,С��������,�뵡,��˯,����Ƥë,צ��Ӧ��ľ,�ж�Ϊ����.
����ÿ�ܲⶨС�����������仯���,����С����ʱ�ʼ�.��ͣҩ���1��͵�14��,���������ȡ10ֻ��Ѫ,EDTA�����ο���,������Sysmex F2820��ȫ�Զ�Ѫ��������Dzⶨ��ϸ��������ϸ���������ܰ�ϸ����ѪС������Ѫ�쵰����.��ͣҩ���1��͵�14��,ÿ�������ȡ10ֻ��Ѫ,����Ѫ��,���Լ��вⶨ�Ȳ�ת��ø����������ø�����ص����������ܵ��ס����ס�Ѫ�Ǻ���.��ͣҩ���1��ÿ�������ȡ3ֻ,ͣҩ���14���ʼ�ʣ��С����,�ɼ��ġ��Ρ�Ƣ���Ρ���,��������ϵ��.���ʼ췢���в����仯������,���в�����֯ѧ�۲�.
����2��������
����2.1���Զ�������
��������1�ι��"�ٿ��ⶾ�ڷ�Һ"��,��������С�����δ����������,����ʽ���������ܼ�������Ƽ��İ���������(LD50).�ý������,"�ٿ��ⶾ�ڷ�Һ"��LD50>16 000mg/kg,��ҩ�ﶾ�Էּ���,����Ϊ��ҩ����.
����2.2����ҩ���IJⶨ
������������ҩ�걨���Ϲ淶,δ�ܼ���LD50�IJ�Ʒ�迪չ����ҩ������.��������ҩ�������鷽��,��40.0g/kg�������ι���ٿ��ⶾ�ڷ�Һ��,����С���������ڽ���,�����,��������С���������ˮ�Ͳ�ʳ��תΪ����,7d������С������������.ͬʱ,������������С����,�ʼ����ࡢ���ࡢƢ�ࡢ���ࡢ����,���۹۲��δ���쳣�仯,��Ϲ۲�����֪,С���������ҩ��(MTD)Ϊ40.0g/kg,�൱���ٴ���ҩ��(0.1g/kg)��400��,˵������������ʹ��"�ٿ��ⶾ�ڷ�Һ"��������.
����2.3�����Զ�������
����2.3.1ҩ���С����һ��֢״��Ӱ��
��������3 200��1 600��800mg/kg�ļ���������С����ÿ�쾭�ڹ�θ��ҩ1��,����30d,�������ڶ������������С�����δ�۲쵽���Ե��쳣��Ӧ���ж�֢״,��ʳ����ˮ�������ŷ������,���������������,���ݱ��ж���������Ϊ��.
����2.3.2 ����ҩ���С����ѪҺ����ָ���Ӱ��
�����ɱ�1��֪,������ҩ30d��,"�ٿ��ⶾ�ڷ�Һ"�ߡ��С��ͼ������С����Ѫ����ָ�����������Ȳ����������(P>0.05),����,"�ٿ��ⶾ�ڷ�Һ"��С����Ѫ�쵰�ס���ϸ������ϸ����ѪС���δ��������Ӱ��.
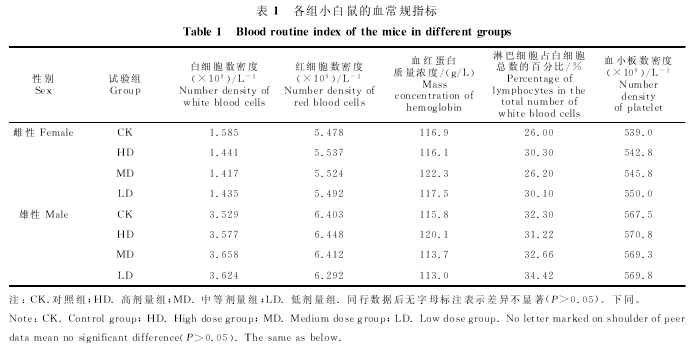
����2.3.3 ����ҩ���С����ѪҺ����ָ���Ӱ��
�����ɱ�2��֪,������ҩ30d��,"�ٿ��ⶾ�ڷ�Һ"�ߡ��С��ͼ������С����ѪҺ�����л��ص�����ָ�����������Ȳ����������(P>0.05).˵������ҩ���С����ĸ��ࡢ���������Ӱ��.
����2.3.4 ����ҩ���С���������ϵ����Ӱ��
����ͣҩ���1��͵�14����ʼ�����ʾ,����С�����ġ��Ρ�Ƣ���Ρ�������̬����ɫ���ʵؾ�����,���������ۿɼ�����,�����С��������ࡢ���ࡢƢ�ࡢ���ࡢ���ࡢ����ϵ�������������(P>0.05)(��3).˵��,����ʹ��"�ٿ��ⶾ�ڷ�Һ"���ᵼ�¶���ʵ���������˻��쳣�仯.
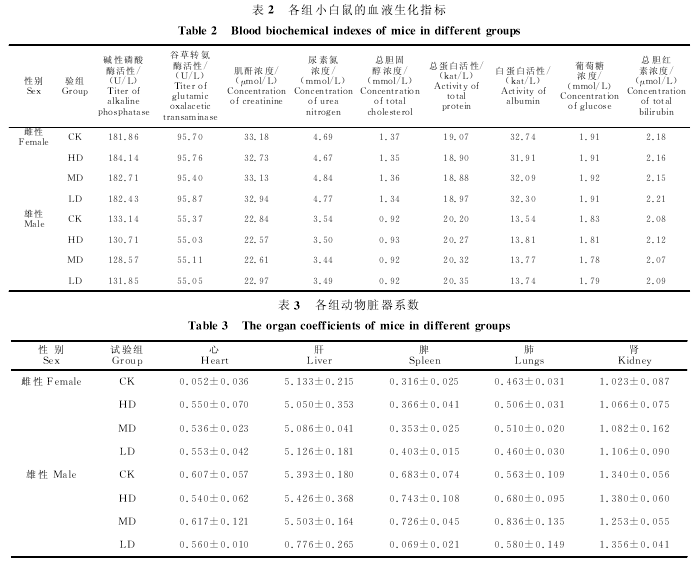
����3�� ��
����3.1"�ٿ��ⶾ�ڷ�Һ"�ļ��Զ�������
�������Զ���������ȷ���ж����÷�ʽ���ж���Ӧ,�Լ�Ϊ�Ǽ��Ժ����Զ�������۲�ָ�꼰���������ṩ�ο�����Ҫ����,Ҳ����ҩ���ﰲȫ���۵���Ҫָ��[10].��������,���Զ�����������"�ٿ��ⶾ�ڷ�Һ"��Һ����Ũ�Ⱥ������Ӱ��,�����趯����������ҩ��,���������������LD50.����ҩ�ﶾ�Էּ���,LD50>16 000mg/kgʱ,ҩ�����ΪΪ��.�����й�����ҩ�з��淶���걨ָ��,�������LD50��ҩ�������������ҩ��,һ����ﵥ�λ�24h��2~3�η���������ҩ���ķ�Ӧ[11].��������,С���ξ��ڹ������Ϊ40.0g/kg��"�ٿ��ⶾ�ڷ�Һ"��,һ�����������,δ����������,�ʼ�������δ�������쳣�ı�.�����ٴ�����ʹ��ҩ�ﲻ��ж�����ɲ�������Ӱ��,"�ٿ��ⶾ�ڷ�Һ"����ҩ���ɶ�Ϊ40.0g/kg.
����3.2"�ٿ��ⶾ�ڷ�Һ"�������Զ�����
�������о�ѡ������ж����Ľ���С������Ϊ���鶯��,�Կ���"�ٿ��ⶾ�ڷ�Һ"�����Ƿ���ж������ü��䶾�����õ�ǿ��.С����30dι������������ҩ�����������Σ������Ҫ����,��������ҩ���������Ũ����Һ�Ʊ�������,ѡ��3 200��1 600��800mg/kg 3��������,�ֱ��ǰж����Ƽ�����(0.4g/kg)��8��4��2��,�ﵽ�������Ҫ��.��������ʾ,3��������С�����ѪҺ���桢ѪҺ����ָ�ꡢ����ϵ����������������Ų���(P>0.05),������������֯����ѧ�쳣�仯.�����ں����Ƴ̷�Χ��,ҩ��"�ٿ��ⶾ�ڷ�Һ"��������Զ���������ԵĶ�������.
����4�� ��
����С�����Զ��������С���������Զ�������������,�ٿ��ⶾ�ڷ�Һ��������;���ٴ��Ƽ�����ʹ���ٿ��ⶾ�ڷ�Һҩ���ƶ������ж�,��ȫ�ɿ�,�Զ��������������,������ҽ�ٴ��ƹ�Ӧ��.
����Reference(�����):
����[1]YANG Xianpeng(������),HAO Baocheng(�±���),LI-ANG Jianping(����ƽ),et al.Research advances in the de-toxificating preparation of swainsonine in"Locoweed"andits application to anti-tumor[J].Journal of Anhui Agri Sci(����ũҵ��ѧ),2012,40(5):2664-2665,2668(in Chinesewith English abstract).
����[2]XIANG Meng(����),SHI Guangliang(ʯ �� ��),LUYangang(³�Ӹ�),et al.Acute toxicity of total alkaloids ofAmmopiptanthus mongolica seeds to mice[J].Journal ofGansu Agricultural University(����ũҵ��ѧѧ��),2012,47(1):49-52(in Chinese with English abstract).
����[3]LEI Hongdong(�궫),LIANG Jianping(����ƽ),GUOZhiting(��־͢),et al.Study on the acute toxicity of Di-chroa febrifugaextractive[J].China Animal Husbandry& Veterinary Medicine(�й�������ҽ),2011,38(6):236-238(in Chinese).
����[4 CHEN Yi(� D),CHEN Chao(�³�).Subchronic oraltoxicity study of Daohuaxiang Vigor Liquor(DVL)in wist-ar rats[J].Liquor-Making Science & Technology(��ƿƼ�),2008(8):43-46(in Chinese with English abstract).
����[5]SHI Dongxia(ʯ��ϼ),JIANG Zhongrong(������),YINZhongqiong(������),et al.Studies on the subchronic oraltoxicity of neem oil in mice[J].Chinese Veterinary Science(�й���ҽ��ѧ),2011,41(1):79-84(in Chinese with Eng-lish abstract).
����[6]LIU Hongmei(�� �� ÷),ZHENG Aihua(֣ �� ��),CAIGuangxian(�̹���).Long-term toxicity testing of ChaoweiSini Decoction on rats[J].Chinese Archives of TraditionalChinese Medicine(�л���ҽҩѧ��),2012,30(4):776-779(in Chinese with English abstract).
����[7]QU Falin(�ķ���),GUO Wei(��ΰ),SUN Yuanqi(��Ԫ��),et al.Study on acute toxicity test of Rukang oral liquid[J].Journal of Strait Pharmaceutical(��Ͽҩѧ),2012,24(1):32-34(in Chinese with English abstract).
����[8]YUAN Bojun(Ԭ����),LIAO Mingxu(������),LI Bo(�).Drug toxicology experiment method and technology(ҩ�ﶾ��ѧʵ�鷽���뼼��)[M].Beijing:Chemical In-dustry Press,1997(in Chinese).
����[9]ZHU Beilei(�� �� ��).Animal Toxicology(�� �� �� �� ѧ)[M].Shanghai:Shanghai Scientific and Technical Publish-ers,1989(in Chinese).
����[10]XU Shuyun(������),BIAN Rulian(�����),CHEN Xiu(����).Methodology of Pharmacological Experiment(ҩ��ʵ�鷽��ѧ)[M].Beijing:People's Medical Pub-lishing House,2005(in Chinese).
����[11]WANG Dongsheng(������),XIE Jiasheng(л����),LIShihong(������),et al.The acute toxicity of Gongyijingtincture[J].Hubei Agricultural Sciences(����ũҵ��ѧ),2011,50(2):346-352(in Chinese with English abstract).





