
药物不良反应( ADR) 是指与治疗目的无关的药物作用[1]。自 2011 年重新修订的《药品不良反应报告和监测管理办法》颁布以来,我院也相应调整了药品不良反应报告和监测的管理,组织开展了相关专业人员的宣传和培训工作。本文对我院 ADR 报告进行回顾性调查,总结分析 ADR 发生的特点及规律,为改进我院 ADR 报告和监测工作及临床合理用药提供参考。
1 资料与方法
1. 1 一般资料 收集本院普爱院区各临床科室 2012至 2013 年填写的 155 例 ADR 报告表。
1. 2 方法 整理资料后将患者年龄、性别、既往 ADR史、给药途径、涉及药品种类、累及器官或系统及临床表现、关联性评价、ADR 报告类型及转归等信息录入Excel 软件进行统计分析。
2 结果
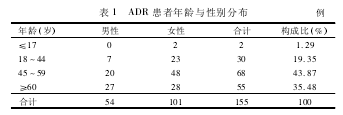
2. 1 ADR 患者一般情况 155 例 ADR 报告中,男 54例( 34. 84%) ,女 101 例( 65. 16%) ,各年龄段人群均有 ADR 发生。既往有药物 ADR 史者 7 例( 4. 52%) ,无 ADR 史者 94 例( 60. 64%) ,ADR 史不详者 54 例( 34. 84%) 。见表 1。
2. 2 ADR 给药途径分布 引起 ADR 的给药途径以静脉给药最为常见,达到 125 例,占 80. 65%; 其次为口服给药 15 例,占 9. 68%; 外用给药 8 例,占 5. 16%;皮下注射给药 6 例,占 3. 87%; 肌内注射给药 1 例,占0. 64% 。
2. 3 ADR 涉及药品种类分布 155 例 ADR 报告共涉及药品 12 类 63 个品种,其中抗肿瘤药物引发的 ADR位居首位,其次为抗感染药物。见表 2、3。
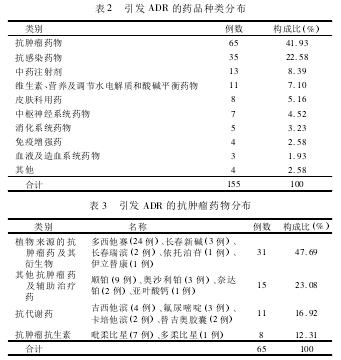
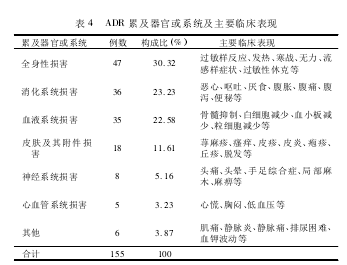
2. 4 ADR 累及器官或系统分布及主要临床表现 我院报告的 155 例 ADR 累及多个器官或系统,以全身性损害、消化系统损害及血液系统损害多见。见表 4。
2. 5 ADR 关联性评价 根据国家药品不良反应监测中心发布的 ADR 关联性评价标准,155 例 ADR 报告中评价为“肯定”75 例( 48. 39%) ,“很可能”63 例( 40. 65%) ,“可能”14 例( 9. 03%) ,“待评价”3 例( 1. 93%) 。
2. 6 ADR 报告类型及转归结果 155 例 ADR 中属于已知的一般反应135 例( 87. 10%) ,新的不良反应9 例( 5. 81%) ,11 例为严重的不良反应( 7. 09%) 。经过停药或对症治疗等处理后,96 例( 61. 94%) ADR 患者痊愈,58 例好转( 37. 42%) ,未好转 1 例( 0. 64%) ,无后遗症及死亡病例。
3 讨论
本院 2012 至 2013 年填写的 155 例 ADR 报告中,男女比例为 1∶ 1. 87,女性明显高于男性,可能与我院就诊人群中女性患者比例高有关。由表 1 可知,ADR可以发生于任何年龄段人群,但 45 ~59 岁的中年患者所占比例最大,达到 43. 87%,其次为 60 岁以上的老年患者,占 35. 48%,提示中老年患者是我院发生 ADR的高风险人群,由于许多器官的储备功能明显下降,对处置药物的能力和对药物反应上与青年人有明显差异,加之合并用药种类增多以及对医生处方的依从性差,因而 ADR 的发生率高[2]。
引发 ADR 的给药途径主要为静脉注射给药( 80. 65%) ,静脉给药使药品直接进入血液,不经过消化道及肝脏防御系统的处理,引起的不良反应远高于口服给药等其他给药途径。另外,药物的 pH 值、渗透压、微粒、内毒素等均可能成为引发不良反应的因素,同时注射剂的制剂质量与药品不良反应发生的关系也较为密切[3]。建议临床医师应坚持正确的用药原则,考虑药物的理化性质及药动学特点,根据病情采用适当的药物剂型和给药途径,在静脉用药初期医务人员应密切监护患者状况、控制滴注速度,及时预防和处理ADR 的发生。
从涉及药品分布看,我院引发 ADR 的药品种类主要为抗肿瘤药物和抗感染药物,临床表现主要为全身性损害( 30. 32%) 、消化系统损害( 23. 23%) 及血液系统损害( 22. 58%) ,这与上述两类药物的大量使用有关。抗感染药物历年来一直排名国内 ADR 报告[2 -4]数量首位,在我院 ADR 报告中临床表现以过敏样反应等全身性损害最为常见,但所占比例有下降趋势。我院普爱院区为湖北省特色肿瘤专科医院,近年来抗肿瘤药物引起的 ADR 报告逐年增多,临床表现以消化系统及血液系统损害多见,特别是植物来源的抗肿瘤药及其衍生物增加迅速,其所含有效成分复杂、质量标准低、可控性差,不溶性微粒易导致静脉炎及过敏反应[5]。目前我院用量较大的植物来源抗肿瘤药物主要为多西他赛,在 65 例抗肿瘤药物 ADR 报告中多西他赛占24 例,其中18 例为骨髓抑制( 包括4 例严重不良反应) ,3 例消化系统损害,1 例低血压,1 例发热,1例脱发。多西他赛不良反应的另外一个特点就是以女性患者居多( 20 例) ,这可能与多西他赛的抗癌谱有关,因其主要用于治疗乳腺癌和宫颈癌,但亦不排除医生的用药习惯[6]。
根据我院就诊患者的人群及用药特点,在坚持抗感染药物的合理使用及监测的同时,应针对抗肿瘤药物完善监测管理制度,临床医药人员应高度重视抗肿瘤药的潜在危险,充分了解可能出现的不良反应,用药前应综合考虑患者年龄、病情、过敏史、药物特性及配伍禁忌等因素制定个性化给药方案,化疗期间应严密监测患者血液学指标变化随时调整用药剂量与疗程,同时做好针对性的防治措施,最大限度地控制和减少ADR 发生。
参考文献:
1 陈新谦,金有豫,汤光主编. 新编药物学. 第 17 版. 北京: 人民卫生出版社,2011. 25.
2 安泽余,殷玉会,顾吉顺. 我院 290 例药品不良反应报告分析. 河北医药,2012,34: 1252-1253.
3 牟洪. 我院 2008 年和 2009 年药品不良反应监测报告分析. 中国药业,2011,20: 41-43.
4 李艳. 我院药物不良反应报告分析. 河北医药,2013,35: 3002-3003.
5 李蓉,董志,路晓钦,等. 重庆市 818 例抗肿瘤药不良反应报告分析.中国药房,2013,24: 3225-3227.
6 徐艳艳,冯平,郭小红. 25 例多西他赛严重不良反应报告分析. 药物流行病学杂志,2012,21: 388-390.





