氯胺酮( ketamine)俗称“K粉”,镇痛药类,由美国药剂师Stevens于1962年首次成功合成,后被用于战争创伤外科手术麻醉药及临床手术麻醉剂或麻醉诱导剂 ;因其具有致幻作用,在世界范围内被广为滥用。在我国,氯胺酮的滥用日趋严重,尤其在一些歌舞厅等娱乐场所较多见,使用群体以青少年为主,滥用方式主要经鼻、口吸食,通常与海洛因、大麻等毒品合并使用。用鼻吸食氯胺酮吸收、起效快,一般在5~10 min内起效,在鼻、口腔黏膜及大脑等高灌注组织中氯胺酮含量较高[1],人体内氯胺酮代谢半衰期为2~4 h.目前,国内外对人体血液、尿液和头发中新型毒品氯胺酮的检测方法有一定研究,通常采用GC/MS法[2-6]、LC-MS/MS法[7-13],其中以LC-MS/MS法检测为主,而对唾液中氯胺酮的检测方法文献报道仍然较少。本文采用超高效液相色谱-串联质谱法对唾液中氯胺酮的定性定量检测方法进行了研究。
1 材料与方法
1.1仪器与试剂超高效液相色谱-串联质谱仪,配Agilent 1290型超高效液相色谱仪(Analyst?software工作站)和AB SCIEX 4000Q TRAP串联质谱仪,电喷雾离子源(ESI)。
氯胺酮购自公安部物证鉴定中心 ;化学试剂乙腈、甲醇为色谱纯,甲酸、氨水为分析纯,实验用水为屈臣氏去离子水。
1.2实验样品
35份唾液样品均采自云南氯胺酮滥用者。
1.3方法
1.3.1 分析条件
色谱条件 :安捷伦C18色谱柱(2.1 mm×50 mm,1.8μm );流动相A为乙腈,流动相B为0.1 %氨水溶液 ;洗脱梯度 :0~1 min流动相A为1 %;1~2 min流动相A由1 %升到90 %;2~2.5 min流动相A为90 %;2.5~3.5 min流动相A由90 %降到1 %,3.5~6min流动相A为1 %.进样体积5μL;流速0.4 m L/min;运行时间6.01 min;柱温35℃。
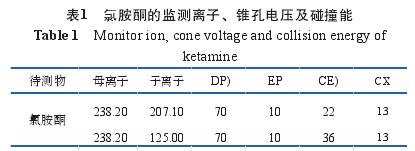
质谱条件 :电喷雾离子源(Turbo Spray)采用正离子扫描,多反应监测(MRM),三重四极杆检测器;毛细管电压为5.5 k V;离子源温度为300℃。氯胺酮的监测离子及锥孔电压、碰撞电压等参数如表1所示。
1.3.2 样品处理
取唾液加适量甲醇并稀释至一定倍数,经振荡3min、超声10 min、离心5 min,取上清液过有机滤膜(13mm×0.22μm)后供检。
1.3.3 标准品工作溶液的配制
使用1.0 mg/m L氯胺酮标准品经稀释得到100.0、50.0、25.0、10.0、5.0、1.0 ng/m L的标准工作液,置4℃冰箱保存。
2 结果与讨论
2.1系统适应性试验
在前述检测条件下,分别对空白唾液、空白唾液添加和氯胺酮滥用者唾液样品进样分析,以238.20/207.10和238.20/125.00两个离子对、保留时间(tR=2.01 min)和已知氯胺酮标准物质比对进行定性,阴性对照无干扰 ;结果表明UPLC-MS/MS检测方法专属性好。氯胺酮的色谱图如图1所示。
2.2流动相的选择
本文分别用0.1 %甲酸的乙腈-0.1 %氨水溶液(A)、乙腈-0.1 %氨水溶液(B)、乙腈-0.1 %甲酸溶液(C)和乙腈-0.3 %甲酸溶液(D)四种流动相对空白添加溶液(25 ng/m L)进行梯度洗脱,经UPLC-MS/MS法进样分析。结果表明 :氯胺酮在碱性流动相乙腈-0.1 %氨水溶液中响应度最高。因此,本文选用乙腈-0.1 %氨水溶液作为流动相。
2.3线性范围、检出限和定量限
将氯胺酮标准品工作液添加至空白唾液中,按1.3.2方法处理成浓度分别为1.0、5.0、20.0、25.0、50.0、100.0 ng/m L系列浓度的空白添加溶液,按1.3.1条件检测;采用Multi Quant 2.1软件中Quqntitate组件,以定量离子(238.20/125.00)峰面积A为纵坐标,质量浓度C为横坐标作图,求得标准曲线的线性回归方程为A=24000C+3320,r=0.9990,氯胺酮在1~100ng/m L范围内线性关系良好。检出限(LOD)为0.06ng/m L(以信噪比S/N大于3为评价标准),定量限(LOQ)为0.21 ng/m L(以信噪比大于10为标准)。
2.4回收率、基质效应、准确度和精密度
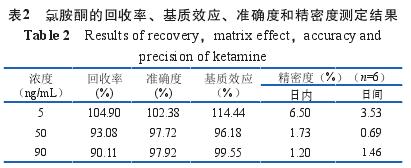
将氯胺酮标准品工作液添加至空白唾液中,按1.3.2方法处理成浓度分别为5.0、50.0、90.0 ng/m L的空白添加溶液,平行操作6份,在1.3.1条件下对以上三种工作溶液进样分析(n=6)。计算回收率和基质效应。一日内连续测定6次,每次间隔2 h,计算日内精密度 ;连续测定6天,每天测定一次,计算日间精密度。如表3示 :唾液样品中氯胺酮的提取回收率、基质效应、准确度和日内、日间精密度分别在90 %~105 %、96 %~115 %、97 %~103 %和0~7%范围内。结果表明,该检测方法具有良好的准确度、精密度、提取回收率和较低的基质效应(见表2)。
2.5稳定性
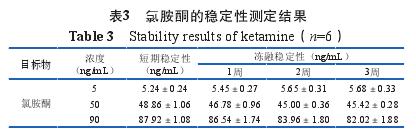
将氯胺酮标准品工作液添加至空白唾液中,配制成一定浓度的低、中、高3种基质加标溶液,室温放置24 h及经过3次冻融循环后,按1.3.2方法处理基质加标唾液成浓度分别为5.0、50.0、90.0 ng/m L的基质加标溶液(n=6),并在1.3.1的实验条件下测定,考察其短期稳定性及解冻稳定性。结果表明,氯胺酮在上述条件下均稳定(见表3)。
2.6实际唾液检测
用UPLC-MS/MS法分别对35份氯胺酮滥用者的真实唾液样品进行检验分析,检出氯胺酮含量低于1μg/m L样品6例,含量在1μg/m L至100μg/m L之间的样品1例,含量高于100μg/m L的样品24例;未检出氯胺酮的样品4例;检出率88.6 %.结果表明:氯胺酮滥用者的唾液中,氯胺酮的检出率高,且含量比较高。分析者认为,唾液中氯胺酮含量的差异可能与氯胺酮的摄入方式、摄入量及唾液采集时间有关,尤其是吸食氯胺酮时,其唾液中氯胺酮的含量往往较高,因为唾液中的淀粉酶不能水解氯胺酮,因此能检测出氯胺酮原体。
3 结论
本文选用甲醇蛋白沉淀法处理唾液样品中的氯胺酮,具有提取回收率高、基质效应好、处理操作简便等优点,适用于唾液样品中氯胺酮的提取、分离。分别考察了碱性流动相、酸性流动相等多种流动相对氯胺酮色谱质谱行为的影响,结果表明氯胺酮在碱性流动相中色谱行为好、响应度高,故选用碱性流动相对氯胺酮进行梯度洗脱。本文建立的超高效液相色谱-串联质谱法操作简便、快速、灵敏度高,可作为吸毒检测工作中对氯胺酮检测的一种新方法。
参考文献
[1]刘小兴,熊勇华。氯胺酮检测研究进展[J].中国公共卫生,2007,23(5):629-631.
[2]邸玉敏,朱军,常靖,等。 GC/MS、GC/NPD法检测血液中氯胺酮[J].中国法医学杂志,2010,25(3):169-171.
[3]常崇佐。气相色谱 - 质谱联用检测唾液中氯胺酮[J].分析仪器,2010(6):26-29.
[4]朱军,邸玉敏,常靖,等。 GC/MS、GC/NPD法检测毛发中的氯胺酮[J].中国法医学杂志,2013,28(3):184-187.
[5]SO P K, NG T T, Wang H X, et al. Rapid detection and quan-titation of ketamine and norketamine in urine and oral fluid bywooden-tip electrospray ionization mass spectrometry[J]. TheAnalyst: The Analytical Journal of the Royal Society of Chem-istry, 2013, 138(8):2239-2243.
[6]LIAN K, ZHANG P, NIU L, et al. A novel derivatization ap-proach for determination of ketamine in urine and plasma bygas chromatography-mass spectrometry[J]. Journal of chroma-tography, A, 2012, 1264(22):104-109.
[7]高秀蓉,刘莉。 UPLC-TOF/MS法检测减肥中药制剂中的盐酸氯胺酮[J].华西药学杂志,2012,27(4):467-468.
[8]翟 晚 枫, 张 春 水, 高 利 生, 等。液 相 色 谱 - 质 谱 联 用同时检测17种常见毒品的定性分析方法[J].刑事技术,2014,(3):24-25,32.
[9]HARUN N, ANDERSON R A, CORMACK P A, et al. Analysisof ketamine and norketamine in hair samples using molecularlyimprinted solid-phase extraction (MISPE) and liquid chroma-tography-tandem mass spectrometry (LC-MS/MS)[J]. Analyti-cal and bioanalytical chemistry, 2010, 396(7):2449-2459.
[10]ZHU K Y, LEUNG K W, TING A K, et al. The establishment ofa highly sensitive method in detecting ketamine and norketaminesimultaneously in human hairs by HPLC-Chip-MS/MS[J]. Fo-rensic science international, 2011, 208(1-3):53-58.
[11]NETTO J D, MAKER G C, MAKER G L,et al. Liquid chroma-tography tandem mass spectrometry for the simultaneous quanti-tative analysis of ketamine and medetomidine in ovine plasma[J].Biomedical Chromatography, 2011, 25(12):1374-1380.
[12]NEMA T, CHAN E C, HO P C, et al. Extraction of ketaminefrom urine using a miniature silica monolithic cartridge followedby quantification with liquid chromatography tandem mass spec-trometry (LC-MS/MS)[J]. Journal of separation science, 2011,34(9):1041-1046.
[13]TSUI T K, CHAN A S, LO C W, et al. Performance of a point-of-care device for oral fluid ketamine evaluated by a liquidchromatography-tandem mass spectrometry method[J]. Journalof Analytical Toxicology, 2012, 36(3):210-216.