全球有 3. 5 亿人感染乙肝病毒( hepatitis B virus,HBV) ,感染 HBV 是肝脏疾病的主要原因,HBV是肝细胞癌( hepatocellular carcinoma,HCC) 的致病因子已得到公认。肿瘤的扩散、转移是恶性肿瘤的主要特征,肝癌细胞的连续增殖和不断分化是肝癌转移浸润的重要原因之一。基质金属蛋白酶( matrixmetalloproteinases,MMP) 是一种依赖锌离子的蛋白酶家族,在肿瘤的转移浸润过程中参与细胞外基质的降解。其中 MMP-2 与肝癌的发生发展、转移浸润密切相关。HepG2. 2. 15 细胞是含有 HBV 基因的肝癌细胞,是研究 HBV 的细胞模型系统。HBx基 因是HBV病毒基因组中最小的开放性读码框,HBx 蛋白是一种多功能蛋白,参与细胞周期与凋亡调控、信号转导通路、DNA 复制、细胞黏附和肝癌发生等病理过程。有研究显示肝细胞在表达 HBx 后MMP 的表达也会发生改变,具体机制还有待进一步研究。本实验应用 RNA 干扰技术沉默 HBx 基因,观察抑制 HBx 基因表达对 HepG2. 2. 15 细胞增殖及MMP-2 表达的影响,初步探讨 HBx 基因与肝癌转移浸润的相关性。
1 材料和方法
1. 1 材料 肝癌细胞株 HepG2. 2. 15 购自博慧斯生物技术公司; psiHBV/X 与对照质粒 pTZU + 1 由泸州医学院张建军教授惠赠; 质粒扩增菌种 DH5α、内切酶等购于宝生物有限公司; DMEM 高糖培养基、胰蛋白酶为 Gibco 产品; 胎牛血清购于HyClone 公司; LipofectamineTM2000 为 Invitation 公司产品; MMP-2抗体购自 Santa Cruz 公司; PCR 引物由 TakaRa 公司合成。
1. 2 方法
1. 2. 1 实验分组及质粒转染 实验分四组: 以未转染的细胞作为空白对照组( control group) ; 仅加脂质体的细胞作为脂质体组( LipofectamineTM2000 group) ; 以转染阴性对照质粒细胞作为质粒对照组( control plasmid group) ; 以转染 psiHBV/X 质粒细胞作为 psiHBV/X 实验组( psiHBV/X group) 。利用脂质体 LipofectamineTM2000 将 pTZU + 1 与 psiHBV / X 质粒转入细胞( 操作步骤同说明书) : 选取对数生长期细胞,待细胞汇合度为70%左右时进行转染,6 h 后更换正常培养基,继续培养24、48、72 h。
1. 2. 2 RT-PCR 检测 HBx 基因的表达 RT-PCR 分析转染24 h后各组细胞 HBx 基因的表达情况,HBx 引物为: 上游5'-TCATCGCCAGCATCATCAAAC-3',下游 3'-ATGTACGGCTG-GAGGTCTGTCA-5',扩增长度为 463 bp。用 RNA 抽提试剂盒分别提取每组细胞总 RNA,按试剂盒说明书进行反转录反应,以 2 μL RT 产物为模板,分别扩增 β-actin 和 HBx 基因片段。扩增产物行琼脂糖凝胶电泳,用凝胶成像系统扫描,以各组目的基因与内参的吸光度比值作为相对表达量,比较各组之间的差异。
1. 2. 3 MTT 法检测细胞的增殖 取对数生长期细胞接种于96 孔板中,1 × 104/ 孔。按实验分组进行细胞转染,置于 CO2培养箱中培养 24、48、72 h,洗掉培养液,加入不含胎牛血清的培养基 100 μL、50 μL MTT 溶液,继续培养 4 h,吸掉各孔上清液,每孔加入150 μL 二甲基亚砜,摇床低速震荡10 min,预热酶联免疫检测仪 20 min 后,酶标仪 490 nm 波长处测定各孔吸光度值,计算转染24、48、72 h 细胞增殖情况。
1. 2. 4 Real-time quantitative PCR ( qRT-PCR ) 检 测 MMP-2mRNA 表达 细胞总 RNA 提取同上。取 RNA 样品 2 μL,用98 μL DEPC 处理过的双蒸水混合于石英比色杯中,以 DEPC 处理过的双蒸水为空白对照管,在紫外分光光度计上分别测定其260 nm 和 280 nm 处的吸光度( A) 值。1. 70≤A260/ A280≤2. 2 认为纯度符合要求。将 RNA 样品用以 DEPC 处理过的双蒸水稀释为50 ng / μL。上反转录仪,反转录条件为: 37℃ 15 min,85℃ 5 s。取出 cDNA 后进行后续实验。MMP-2 引物: 上游 5'-CTCATCG-CAGATGCCTGGAA-3',下游 3'-CAGCCTAGCCAGTCGGATTTG-5',扩增长度为 167 bp。内参 β-actin 引物: 上游 5'-TGGCACCCAG-CACAATGAA-3',下游 3'-CTAAGTCATAGTCCGCCTAGAAGCA-5',扩增片段长度232 bp。采用2- △△Ct法计算 MMP-2 mRNA 的相对表达量。
1. 2. 5 Western blot 法检测 MMP-2 蛋白表达 用预冷 PBS 将各组细胞漂洗 2 次,加入 1 mL 蛋白裂解液充分裂解,4℃,12 000 r / min离心 5 min,上清即为蛋白提取物。按 BCA 蛋白含量检测试剂盒步骤制作标准曲线,计算样品蛋白浓度。取30 μg蛋白样品与上样缓冲液混匀,行SDS-PAGE,80 V 约4 h。电泳完后取下凝胶,电转至PVDF 膜,用50 g/L 的脱脂奶粉室温摇床封闭1 h。兔抗人 MMP-2 抗体 MMP-2 一抗( 1∶500) 37℃孵育 2 h,TBST 洗膜 3 次。加 HRP 标记的山羊抗兔二抗 37℃ 孵育 1 h,TBST 洗膜 3 次,ECL 发光显色。用 Quantity One 定量分析软件分析吸光度比值。
1. 2. 6 统计学分析 实验结果用 x ± s 或 百分比表示,用SPSS18. 0 统计软件包进行分析,多组定量资料比较用方差分析,组间比较用 t 检验。实验结果以 P <0.05 为差异有统计学意义。
2 结果
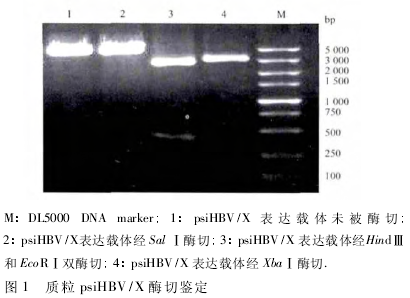
2. 1 质粒 psiHBV/X 酶切、测序 psiHBV /X 为氨苄抗性质粒,经转化 DH5α 后,对从阳性菌落中扩增提取的质粒 psiHBV/X 进行酶切,psIHBV/X 表达载体未被酶切和经 SalⅠ酶切后,大小基本相等,经 Hind Ⅲ和EcoRⅠ双酶切后重组体质粒产生 2 800 bp、395 bp 左右的2 个条带,经 Xba Ⅰ酶切成约 3 100 bp 的 DNA 片段,证实重组表达质粒 psIHBV/X 构建正确( 图 1) 。
将质粒送到生工测序,引物为 U6 启动子的通用引物,测序结果显示 shRNA 的表达模板 5'-TCGAG-GAACCAACAAGAAGATGAG TTCGCTCATCTTCTTGT-TGGTTCTTTTT-3'成功插入了载体中。证实特异表达载体 psiHBV/X 构建正确。psiHBV/X 质粒插入测序结果( 下划线为小干扰 RNA 的作用靶点) : GCTT-TATATATCTTGTGGAAAGGACGAAACACCGTCGA G-GAACCAACAAGAAGATGAGTTCGCTCATCTTCTTGT-TGGTTCTTTTTCTAGAGCGGACTTCGGT。
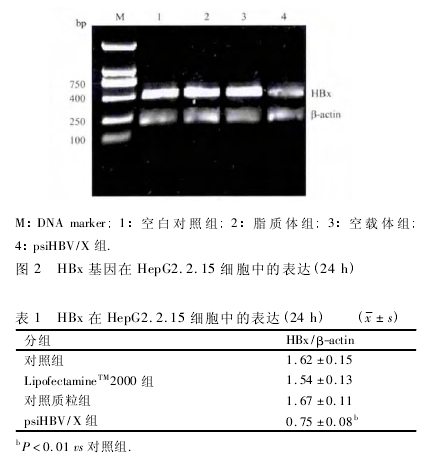
2. 2 RT-PCR 检测 HepG2. 2. 15 细胞 HBx 基因的表达 RT-PCR 检测结果显示 psiHBV/X 组 HBx 表达量低于其它各组,差异有统计学意义( P < 0. 01,图 2、表 1) ,抑制率为 53. 60%。而其他各组表达量差异无统计学意义( P >0. 05) 。
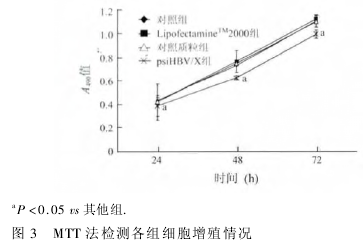
2. 3 psiHBV /X 转染抑制细胞的增殖 MTT 法结果显示: 空白组24、48、72 h A490的吸收值分别为0.44 ±0. 03、0. 73 ± 0. 02、1. 11 ± 0. 05,而 psiHBV / X 组 24、48、72 h A490的吸收值分别为0.39 ±0.09、0.62 ±0.02、0. 99 ± 0. 04。说明 psiHBV / X 组在转染后 24、48、72 h都对细胞生长具有抑制作用,与对照组相比差异有统计学意义( P <0.05,图3) 。
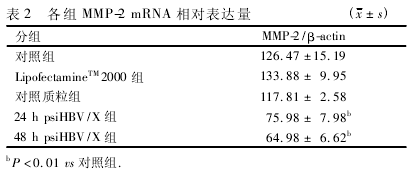
2. 4 psiHBV /X 转染抑制细胞 MMP-2 mRNA 表达标准曲线线性良好,具有可重复性,证明 RNA 有较好的扩增能力。由融解曲线图可知各实验组曲线峰值单一,主峰位置基本一致,无杂峰,说明产物均一。实验结果使用2- △△Ct法进行分析,结果显示: 空白对照组、脂质体组、质粒对照组表达无显着差异( P >0. 05,表 2) ,干扰 24 h 实验组和 48 h 实验组MMP-2 mRNA 的表达较其它组明显下调( P < 0. 01) 。
2. 5 psiHBV /X 转染抑制 MMP-2 蛋白表达 转染24、48 h 后收集各组细胞,提取总蛋白,Western blot法检测转染后各组细胞 MMP-2 蛋白表达变化。结果所示: 空白对照组、脂质体组、空载体组比较,表达无显着差异( P >0. 05) ,干扰 24 h 实验组和 48 h 实验组 MMP-2 蛋白表达下降,与对照组比较差异具有统计学意义( P <0. 05,图 4,表 3) 。
3 讨论
全球有 3. 5 亿人感染 HBV,HBV 是肝细胞癌( HCC) 的致病因子已得到公认。HBx 基因是 HBV病毒基因组中最小的开放性读码框,是 HBV 复制的关键基因。HBx 蛋白是一种多功能蛋白,与甲基转移酶 PRMT1 结合可调节乙肝病毒的转录,并参与细胞周期与凋亡调控、信号转导通路、DNA 复制、细胞黏附和肝癌发生等病理过程,HBx 蛋白可干扰先天免疫的 RIG-I 通路从而影响病毒的复制。HBx蛋白在肝癌的发生发展中起重要作用。HBx 基因转染可加快肝癌细胞周期的进程,促进肝癌细胞生长,使肝癌细胞恶性程度增高。也有研究显示 HBx 可通过上调 HIF-1 的表达,从而促进肿瘤血管生成及转移。因此,HBx 可作为阻断 HBV 感染相关性肝癌发生发展的靶基因。
MMP 能降解 ECM 中的蛋白成分,破坏肿瘤细胞侵袭的组织学屏障,在肿瘤侵袭转移中起关键性作用,从而在肿瘤浸润转移中的作用日益受到重视,被认为是该过程中主要的蛋白水解酶。目前 MMP 家族已分离鉴别出26 个成员,其中 MMP-2 基因位于人类染色体 16q21,由 13 个外显子和 12 个内含子所组成。研究发现,MMP-2 与肝癌、宫颈癌、胶质瘤等多种肿瘤的浸润侵袭有关。另有研究报道丙型肝炎病毒的感染与 MMP-2 的激活有关。但 HBx在肝癌转移浸润中所起的具体作用还需深入研究。
为进一步探索 HBV 感染与肝癌转移浸润的关系及其作用机制,本研究用 HBx 干扰载体 psiHBV/X转染 HepG2. 2. 15 细胞,观察 HBx 基因沉默后细胞增殖情况及对 MMP-2 表达的影响。实验结果显示:
siRNA 表达载体对 HepG2. 2. 15 细胞增殖有明显抑制作用,抑制率明显高于空白对照组、空载体组、脂质体组。同时,空白对照组、空载体组、脂质体组之间的差异无显着性。结果显示在转染后 48 h 抑制效果最佳,72 h 抑制效率下降,其可能原因是 siRNA 的表达载体随着细胞的快速分裂而不断的丢失,从而降低了干扰效率。Real-time PCR 和 Western blot 法检测结果显示,转染 psiHBV/X 后 HepG2. 2. 15 细胞中MMP-2 在基因水平和蛋白水平的表达均下调,且随着时间的推移这种抑制越来越明显,提示沉默 HBx基因后 MMP-2 表达受到抑制,因此推测在 HCC 的转移过程中,HBx 或 HBV 可通过上调 MMP-2 的表达水平而增强肝癌细胞的侵袭能力,也增加了乙肝病毒致癌的可能性。提示 HBx 可作为控制肝癌转移的一个靶基因。
参考文献:
[1] Gearhart TL,Bouchard MJ. The hepatitis B virus HBx proteinmodulates cell cycle regulatory proteins in cultured primary humanhepatocytes[J]. Virus Res,2011,155( 1) : 363 - 367.
[2] Kleiner DE Jr,Stetler-Stevenson WG. Structural biochemistry andactivation of matrix metalloproteinases[J]. Cell Biol,1993,5( 5) :891 - 897.
[3]吴时胜,邵立华,李尚日,等. MMP-9 和 MMP-2 基因多态性与原发性肝癌侵袭转移的关系[J]. 肿瘤防治研究,2012,39( 6) : 683 -686.
[4]Sells MA,Chen ML,Acs G. Production of hepatitis B virus particlesin Hep G2 cells transfected with cloned hepatitis B virus DNA[J].Proc Nati Acad Sci U S A,1987,84( 4) : 1005 - 1009.
[5]催彦芝,罗荣城. 乙型肝炎病毒 X 蛋白与肝癌研究进展[J]. 癌症进展杂志,2007,5( 4) : 324 -328.
[6]陈文豪,王晓茜,李秀金,等. HBx 通过上调前列腺素 E2 受体2的表达增强 HL-7702 肝细胞的侵袭能力[J]. 中国肿瘤临床,2011,38( 24) : 1529 - 1534.
[7]Benhenda S,Ducroux A,Rivière L,et al. Methyltransferase PRMT1is a binding partner of HBx and a negative regulator of hepatitis Bvirus transcription[J]. J Virol,2013,87( 8) : 4360 - 4371.
[8]Kumar M,Jung SY,Hodgson AJ,et al. Hepatitis B virus regulatoryHBx protein binds to adaptor protein IPS-1 and inhibits theactivation of beta interferon[J]. J Virol,2011,85( 2) : 987 - 995.
[9] Feng H,Li X,Niu D,et al. HBx expression activates RhoAGTPase: impact on cell migration[J]. Cell Biol Int,2011,35( 2) :159 - 164.
[10]Jain S,Singhal S,Lee P,et al. Molecular genetics of hepatocellularneoplasia[J]. Am J Transl Res,2010,2( 1) : 105 - 118.
[11]孙爱武,陈园生,李 黎,等. 乙型病毒性肝炎和原发性肝细胞癌[J]. 中国疫苗和免疫,2010,16( 2) : 173 -177.
[12]Ying RS,Zhu C,Fan XG,et al. Heptatitis Bvirus is inhibited byRNA interference in cell culture and in mice[J]. Antiviral Res,2007,73( 1) : 24 - 30.
[13]McClune AC,Tong MJ. Chronic hepatitis B and hepatocellular carcinoma[J]. Clin Liver Dis,2010,14( 3) : 461 -476.
[14]李卫华,缪晓辉,戚中田,等. 乙型肝炎病毒 X 蛋白对肝癌细胞生长的影响[J]. 生物医学工程与临床,2008,12( 3) : 235 -238.
[15]Xie H,Song J,Liu K,et al. The expression of hypoxia-induciblefactor-1alpha in hepatitis B virus-related hepatocellular carcinoma:correlation with patients prognosis and hepatitis B virus X protein[J]. Dig Dis Sci,2008,53( 12) : 3225 -3233.
[16]Zhao X,Zhao Z,Guo J,et al. Creation of a six-fingered artificialtranscription factor that represses the hepatitis B virus HBx geneintegrated into a human hepatocellular carcinoma cell line[J]. JBiomol Screen,2013,18( 4) : 378 - 387.
[17]李海燕,曹励民. 三氧化二砷抑制人肝癌 SMMC-772 细胞侵袭及其机制[J]. 细胞与分子免疫学杂志,2012,28( 12) : 1254 -1257.
[18] Song C,Zhu S,Wu C,et al. Histone Deacetylase ( HDAC) 10suppresses cervical cancer metastasis through inhibition of matrixmetalloproteinase ( MMP) 2 and 9 expression[J]. J Biol Chem,2013,288( 39) : 28021 - 28033.
[19] Mou L,Kang Y,Zhou Y,et al. Neurokinin-1 receptor directlymediates glioma cell migration by up-regulation of matrixmetalloproteinase-2 ( MMP-2) and membrane type 1-matrix metalloproteinase( MT1-MMP) [J]. J Biol Chem,2013,288( 1) : 306 -318.
[20]Li Y,Zhang Q,Liu Y,et al. Hepatitis C virus activates Bcl-2 andMMP-2 expression through multiple cellular signaling pathways[J]. JVirol,2012,86( 23) : 12531 - 12543.